HIV,是導致艾滋病的元凶,從20世紀80年代首次被發現以來的幾十年,全球現存約3700萬HIV感染者。在研究如何治愈的道路上,科研人員從未停止腳步,但是迎來的一直都是挫折和失敗,偶然的治愈案例也難以複製。現在聯用抗逆轉錄病毒藥物雖然可以抑製疾病的進展和增殖,但依舊不能完全根除病毒庫。
但是,病毒庫無法被消滅的魔咒,在2019年7月,第一次被成功解除,天普大學和內布拉斯加大學醫學中心的30多名研究人員成功地從實驗室老鼠的DNA中根除了HIV-DNA病毒庫。
這意味人類多年以來在攻克艾滋病的道路上,終於邁出了一小步。

“我邁出了一小步,但人類邁出了一大步。”——尼爾·奧爾登·阿姆斯特朗
柏林病人的啟示
全球被報導的第一個HIV臨床治愈者——"柏林病人"接受了CCR5缺陷型幹細胞移植後,停藥數年後,其外周血、淋巴組織及其他所有組織中的HIV DNA及RNA,目前的技術手段均檢測不到。
"柏林病人"體內也幾乎不存在針對HIV的免疫反應,柏林病人是目前唯一一位HIV臨床治愈者。由於"柏林病人"的治愈,激起了研究者們期望通過改造幹細胞使其CCR5功能缺陷達到功能性治愈的興趣。
一直以來,到底是什麽導致了"柏林病人"達到功能性治愈存在激烈的爭論。“柏林病人”的治愈,可能是以下原因造成的:
一:因為“柏林病人”的白血病,藏在他細胞裡的HIV病毒都不再潛伏,病毒庫被激活,而進一步的化療摧毀了大部分被激活的病毒的宿主CD4+T細胞,幾乎耗竭了病毒庫。
二:造血幹細胞移植前的射線治療,讓被整合到細胞染色體上的HIV病毒區段脫落,最終被從染色體上剝離,終止了HIV在體內的複製和傳播;
三:“柏林病人”自體的免疫系統功能尚全,在通過抗白血病治療的過程中,絕大部分被HIV感染的細胞被殺滅,CCR5缺陷的造血幹細胞移植後分化擴增,替代了這些被殺滅的細胞,並且激活了其他免疫機制清除了所有的被HIV感染的細胞。
後續也有其他研究者和病人嘗試複製了“柏林病人”的治愈方案,但都在治療結束後的數年內與病人體內再次檢測到了HIV,均宣告失敗。
但是在失敗的案例中,HIV病毒學反彈也得到了一定的推遲

基因編輯CRISPR
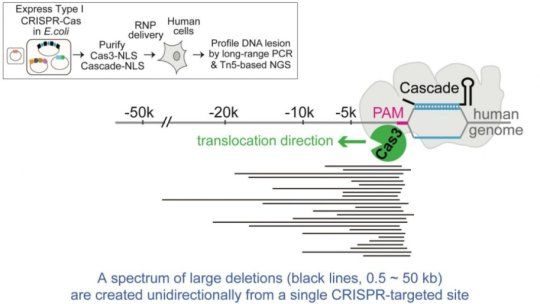
在嘗試複製柏林病人的希望逐漸減小時,科研人員將眼光投向了基因編輯技術。比爾蓋茨投資的生物醫藥公司Editas Medicine,開發出了一種名為CRISPR-Cas9的基因治療法,這種方法旨在利用DNA編輯技術治療多種疾病,這種療法很快就被投入了HIV治療的研究。
CRISPR/Cas系統並不是人類創造的,這個系統在自然界中廣泛存在,其本身為原核生物的免疫系統,使得原核生物用於免疫外來病毒的侵入,同時為細菌提供類似人類免疫應答的獲得性免疫系統,即二次免疫。
在原核生物遭遇病毒入侵後,會產生相應的免疫“記憶”。當再次被同種病毒入侵時,CRISPR系統可以識別出外源基因,並破壞外源基因,免疫病毒對自體基因庫的干擾。(類似於人類遭受病原入侵後,記憶免疫細胞會識別並記住外來病原體的特徵,在再次暴露於同樣病原後,能快速、高效地產生大量抗體或功能性免疫細胞,將病原體清除。)
因其能精準的識別和破壞基因這一特性,CRISPR/Cas系統被改造成為了一種高效的基因編輯工具。CRISPR/Cas9第三代基因組定點編輯技術。CRISPR/Cas9系統也是研究最深入,目前在基因編輯方面應用最廣泛的技術之一。
但是,新技術的應用必定帶來新的隱憂,特別是倫理問題和基因庫汙染。
2018年11月28日,中國科學家賀建奎在香港舉行的人類基因組編輯峰會上發表講話。他進行了一項枉顧倫理的針對雙胞胎基因編輯的實驗。
2015年底,美國NIH仍拒絕資助CRISPR/CAS生殖系編輯療法的研究提案。
2015年12月3日,國際基因編輯峰會發表聲明稱,基因編輯技術禁止被用於修改人類胚胎以建立妊娠。
9隻小白鼠帶來的希望
在基因編輯嬰兒的醜聞風波剛平息不久,我們終於看到在基因編輯技術的應用上對於HIV治療的積極意義。
天普大學和內布拉斯加大學醫學中心於2017年宣布基因編輯技術能大幅度削減小鼠體內的病毒庫,經過改進技術,終於在2019年宣布,人類首次攻克了HIV病毒庫。
此次試驗中,為了確保試驗能正確進行:首先,科研人員改造了小白鼠的免疫系統:在小白鼠出生後,取人類臍帶血分離人CD34+HSC(CD34+造血幹細胞),對小鼠進行肝內注射,移植人類的免疫細胞。確保小鼠免疫系統盡可能與人體等效後,令小鼠感染HIV,在小鼠的肝、脾、腦脊液中,確認存在人類來源的已經感染HIV的CD4+T細胞後展開了試驗。

試驗中製作了DTG、拉米夫定(3TC)和阿巴卡韋(ABC)的前體藥物的緩釋納米晶體,注射進入小鼠體內,用作抗病毒治療。並同時引入CRISPR/Cas9系統,以剪斷HIV逆轉錄完成並整合到CD4+T細胞中的DNA。
在進行試驗的23隻小鼠中,有9隻體內的HIV病毒庫已經完全被清除。

此次試驗的主要參與者,內布拉斯大學的 Howard Gendelman 在試驗聲明中表示,在利用基因編輯的同時,他們製作的DTG、拉米夫定(3TC)和阿巴卡韋(ABC)的前體藥物的緩釋納米晶體也具有重大意義,這種藥物若用於人體,很可能實現每兩個月使用一次藥物,而不是像今天這樣每日使用。而且在進行這個方案時,抗病毒治療是必須的,如果不進行抗病毒治療,CRISPR對病毒庫的破壞速度遠遠達不到病毒庫的擴張速度。如果能減少給CRISPR留下的病毒庫數量,CRISPR成功治愈的可能性就會大大增加。
早發現早治療或成未來治愈的關鍵
從登月,到登陸火星
Gendelman在接受CNN採訪時表示,他們研究小組花了數年時間才確定他們已經清除了HIV病毒,他們檢查了老鼠組織的每一個角落。他說,他們的研究只是第一步,要想找到治愈人的方法還有很長的路要走。
人類比老鼠大得多,如果在人類身上進行該項試驗,科研人員們將不得不面對並處理更多的HIV-DNA病毒庫。而且該方法的安全性和有效性仍待提高,他們將謹慎且積極地繼續進行動物試驗,以期望該方案在靈長類生物身上有效。

Gendelman在接受CNN採訪的最後說到:“我們在月球上留下了第一個腳印,不等於我們現在就能觸及火星。”