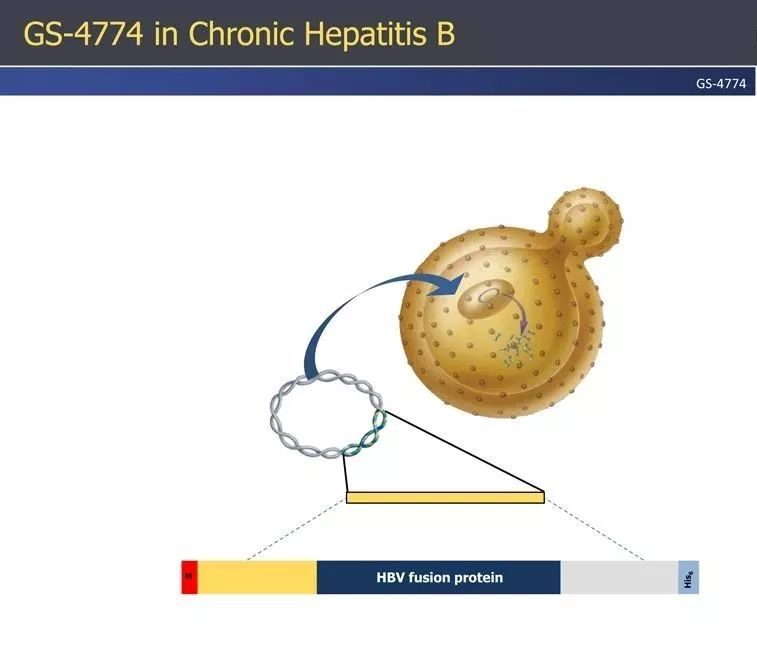
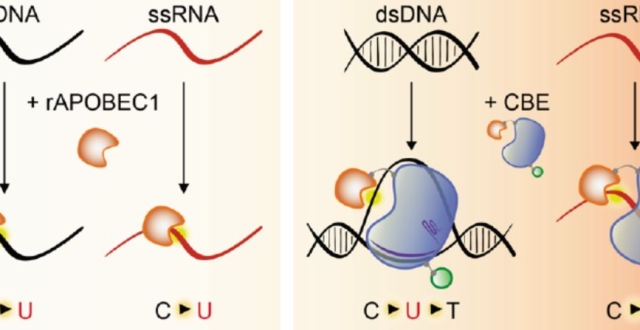
2021年美國肝病研究年會(AASLD2021),研究人員帶來了一種基因編輯技術開發慢B肝新藥的研究進展。2020年,兩位科學家因發明CRISPR/Cas9技術斬獲諾貝爾化學獎,該技術應用於慢B肝前景主要是在直接靶向cccDNA有一定吸引力。

B肝CRISPR/Cas9靶向性,結合抑製DNA修複機制,可顯著增強抗病毒
一、研究背景
研究人員介紹,目前抗B肝病毒(HBV)療法對共價閉合環狀DNA(cccDNA)幾乎沒有影響。B肝病毒能夠使用宿主DNA修複機制,從而進行cccDNA生物合成。我們研究了CRISPR/Cas9技術靶向HBV基因組與抑製DNA修複機制相結合的功效。
二、研究方法
我們設計了靶向HBV基因組的gRNA(HBV-gRNA)和不靶向HBV或人類基因組的對照gRNA(Cont-gRNA)。19天B肝病毒感染後,將串聯 Cas9 和 HBV-gRNA(或 Cont-gRNA)表達載體(HBV-gRNA/Cas9 或 Cont-gRNA/Cas9)慢病毒轉導到 HBV 基因組整合細胞(HepG2.2.15)或原代人肝細胞(PHH)中。
具有可誘導 Cas9 表達的 HBV 易感細胞 (HepG2-hNTCP-iCas9) ,使用單個HBV-gRNA 或 Cont-gRNA 載體進行慢病毒轉導。當HBV 感染後 4 天,Cas9 表達由多西環素 (DOX) 給藥誘導。我們檢查了 CRISPR/Cas9 處理在有或沒有 小干擾RNA(siRNA)抑製DNA修複機制的情況下的抗病毒反應。

三、研究數據
結果表明,Surveyor 檢測顯示,HBV-gRNA/Cas9 的慢病毒轉導誘導了HepG2.2.15 細胞中 HBV-gRNA 靶向的 HBV 基因組區域的插入缺失形成。和Cont-gRNA/Cas9 相比,HBV-gRNA/Cas9轉導可顯著降低HepG2.2.15 細胞上清液中HBVDNA和HBs抗原的水準以及細胞內前基因組RNA(pgRNA)的水準!
同樣,HBV-gRNA/Cas9轉導也降低了上清液中HBVDNA和HBs抗原的水準,以及PHHs 中細胞內pgRNA和cccDNA的水準。下一代測序顯示,HBV-gRNA 轉導和 DOX 誘導的 Cas9 表達,誘導了 HepG2-hNTCP-iCas9 細胞中 HBV-gRNA 靶向的 HBV 基因組區域的插入缺失形成。
HBV-gRNA 轉導,還能夠降低上清液中HBVDNA和HBs抗原的水準,以及HepG2-hNTCP-iCas9 細胞中細胞內 pgRNA 和 cccDNA 的水準。抑製 BRCA 對同源重組至關重要,但並不會改變 CRISPR/Cas9 處理在 HepG2-hNTCP-iCas9 細胞中的功效。
而抑製PARP2或HPF1,對於DNA修複雙鏈斷裂的初始步驟很重要,或LIG4對非同源末端連接 (NHEJ) 也至關重要,它顯著增強了CRISPR/Cas9治療的抗病毒作用。

四、研究結論與開發前景
本研究人員給出的結論是,通過抑製非同源末端連接 (NHEJ) 介導的DNA修複機制,可以增強針對HBV基因組的基因編輯CRISPR/Cas9療法功效。
小番健康結語:這是2021年美肝會上,介紹的一項新型HBV療法,研究人員使用了CRISPR/Cas9技術來靶向B肝病毒的基因組,這種新方法可以通過抑製NHEJ介導的DNA修複,從而增強CRISPR/Cas9療法功效。這項開發技術問世不算久,它還有很漫長的研究之路要走,但CRISPR/Cas9也是目前全球已知的被科學家發現,具有潛在直接靶向B肝病毒複製模板cccDNA的方法!返回搜狐,查看更多
責任編輯: