▎醫藥觀瀾/報導
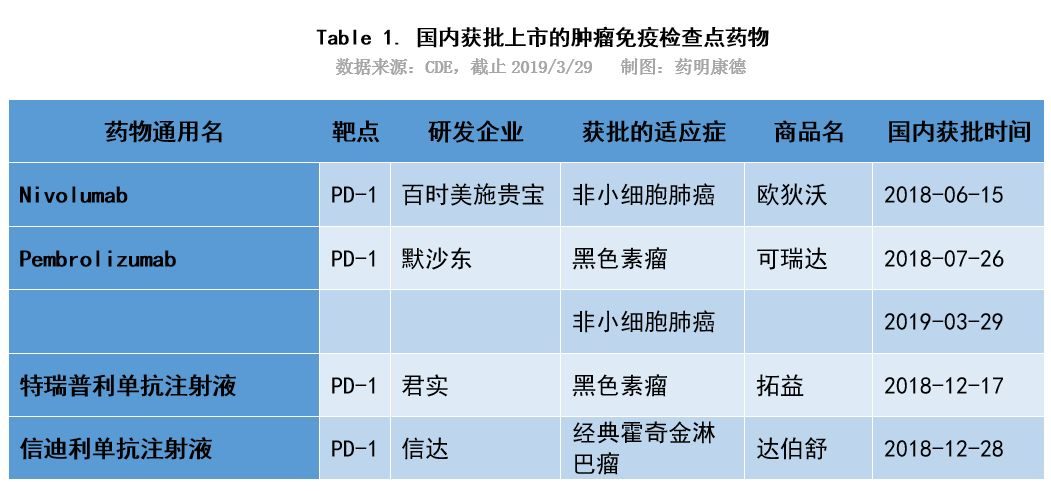
近日,蘇州康寧傑瑞的重組人源化PD-L1單域抗體Fc融合蛋白注射液獲得藥品審評中心的臨床試驗默示許可,擬定適應症為適用於膿毒症及膿毒性休克的治療。這是繼晚期結直腸癌、胃或胃食管結合部腺癌、膽道癌及其他晚期實體瘤等之後,康寧傑瑞PD-L1在中國獲批進入臨床的又一適應症,同時也是該PD-L1在非腫瘤適應症上的首次探索。


根據2018年《中國膿毒症/膿毒性休克急診治療指南》,膿毒症是指因感染引起的宿主反應失調導致的危及生命的器官功能障礙,膿毒性休克定義為膿毒症合併嚴重的循環、細胞和代謝紊亂,其死亡風險較單純膿毒症更高。膿毒症和膿毒性休克是急危重症醫學面臨的重要臨床問題,全球每年膿毒症患者數超過1900萬,其中有600萬患者死亡,病死率超過1/4,存活的患者中約有300萬人存在認知功能障礙。
目前,臨床上的治療方式主要有液體復甦、抗感染治療、血管活性藥物如去甲腎上腺素、糖皮質激素、抗凝治療、腎臟替代治療、機械通氣、鎮靜和鎮痛等。
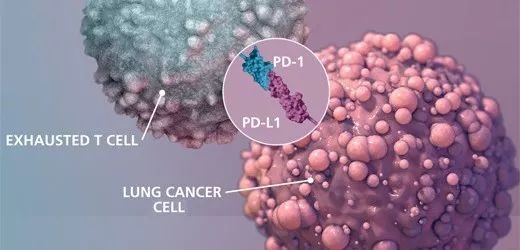
最近的研究表明,在早期高炎症反應狀態下存活的患者,大部分進入免疫抑製階段,更容易繼發感染,增加病死率。程序性死亡分子-1(PD-1)及其配體(PD-L1)是介導機體免疫反應的負性調節因子,在膿毒症的發生發展過程中扮演著重要角色。
近幾年,有關PD-1/PD-L1在膿毒症中的作用受到廣泛關注,無論是在動物實驗還是臨床試驗,抗PD-1/PD-L1抗體均顯示出很好的前景。
此次,康寧傑瑞重組人源化PD-L1單域抗體Fc融合蛋白注射液在膿毒症及膿毒性休克適應症上獲批進入臨床,是PD-L1在非腫瘤適應症上的新嘗試,有望為膿毒症患者帶來新的治療選擇。
根據康寧傑瑞官網,該公司自主研發了一款皮下注射PD-L1抗體新葯(研發代碼KN035),該產品早期開發和臨床前研究由康寧傑瑞完成。2016年2月,康寧傑瑞與思路迪達成在全球範圍聯合開發KN035的合作協議,康寧傑瑞負責臨床樣品和上市後藥品生產,思路迪主導全球註冊、臨床開發和商業化。
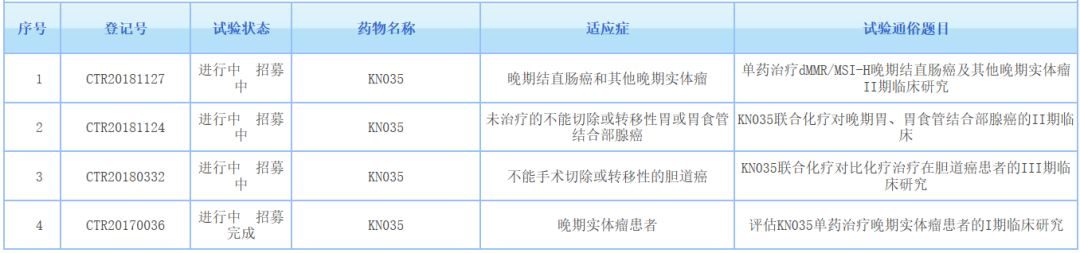
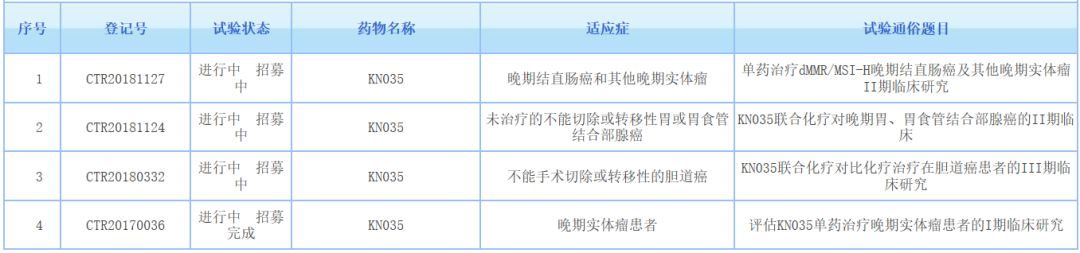
▲KN035國內臨床研究一覽(圖片來源:藥物臨床試驗登記與信息公示平台)
根據康寧傑瑞公告,KN035是目前全球首個進入臨床開發的PD-L1單域抗體,與目前已經上市和在研的PD-(L)1抗體相比有明顯差異化的優勢。KN035具有可皮下注射,常溫下穩定等優點,從而提高病人用藥依從性,改善腫瘤病人生活品質,對實現將腫瘤作為慢性病長期管理的目標具有重要的價值。
目前為止,在美國、日本和中國,先後已有三百多病人參與了KN035的臨床試驗。在中國,KN035已進入臨床後期開發階段,其中針對膽管癌的3期臨床試驗和MSI-H實體瘤的2期臨床試驗已經在中國展開。
歡迎掃碼關注「醫藥觀瀾」微信公眾號,了解更多中國醫藥創新動態。
參考資料:
[1]藥物臨床試驗登記與信息公示平台
[2]藥品審評中心
[3]康寧傑瑞官網