動物模型模型研究,是新藥臨床前研究十分關鍵一步驟,但目前由於全球可用的肝病毒感染模型受到各種限制,多數有代表性的動物研究進展主要還是集中在小鼠方向。許多研究者,試圖建立HBV感染人類肝髒的小鼠模型。

動物模型確定新靶點,B肝代表性進展,主要集於小鼠模型中
由於人類肝細胞嵌合的小鼠免疫缺陷,它們不適合疫苗研究或免疫反應評估。然而,這些小鼠卻是一種很有前途的研究工具,可以用來評估抗HBV藥物和突變株對各種藥物的敏感性。更重要的是,人類肝細胞嵌合小鼠的最大益處是,它們屬於完全重現核HBV cccDNA基因組維護的唯一模型。可以通過這種模型來證明,IFN-α通過表觀遺傳控制cccDNA功能和轉錄的機制,在抑製B肝病毒複製方向的作用。
B肝病毒複製模板,共價閉合環狀DNA(cccDNA)是實現完全根除HBV的重要治療靶點,因此,全球研究人員以闡明控制cccDNA活性分子機制為目的的嵌合小鼠實驗,將更有助於開發更有效的治療方法。但是,由於缺乏HBV和HCV特異性受體分子,小鼠的肝細胞不支持HBV和HCV的進入。瞬態或這兩個人類基因的穩定表達,目前被發現足以允許病毒吸收和支持HBV感染免疫活性的純系小鼠。

這一發現,原則上,近似於策略還可以應用在HBV整個生命周期的小鼠模型生成方向。然而,在B肝病毒感染情況下,雖然牛磺膽酸鹽協同轉運多肽(NTCP)作為B肝病毒的長期功能性受體,全球有研究表明,在小鼠肝細胞NTCP表達式,允許B肝病毒進入但不足以支持HBV感染,建議限制存在的B肝病毒感染小鼠。所以,未來這種基因人源化小鼠方向研究,可能還需要識別上述因素,以求發展具有免疫能力的基因人源化小鼠,並支持HBV感染。
除基因人源化小鼠外,為了在小動物模型中,重現人類對HCV的免疫反應,全球有科學家嘗試開發人類免疫系統和肝組織重組的人源小鼠。簡單的講,這就是擁有人類免疫系統和肝髒組織的人類小鼠,這些小鼠通過基因工程表達FK506結合蛋白(FKBP)和caspase 8的融合蛋白,在白蛋白啟動子(AFC8)的控制下,在肝細胞中具有誘導清除活性作用。

總體上看,全球科學家認為,闡明B肝病毒清除機制更需要建立足夠的小鼠模型,而這些臨床前動物模型數據有望揭示B肝抗病毒藥物新的靶點。前期小番健康也有介紹,B肝病毒感染宿主範圍較窄,在一些缺乏完整免疫應答譜在動物模型研究中,受到相當大的局限性。但是,在動物模型中重現肝髒HBV感染,有助於理解和尋找B肝病毒感染期間,宿主-病毒免疫相互作用的關聯性。

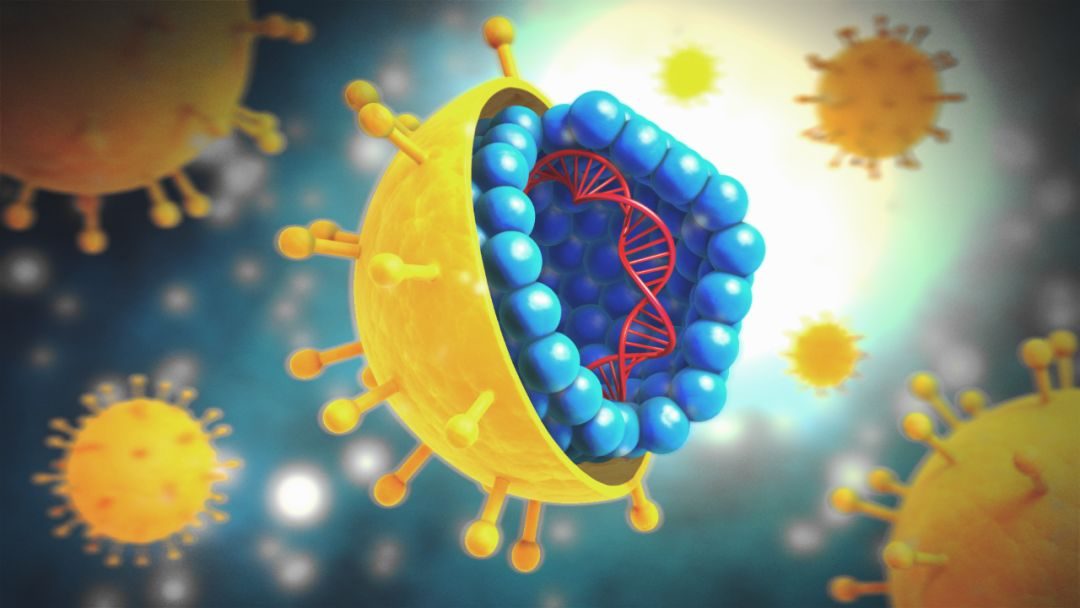
因此,雖然全球已在各種小鼠模型研究積累大量經驗,但還需要進一步建立適合HBV感染的動物模型詳細研究,其一方向是建立一個穩健動物模型來闡明HBV清除機制,找到更優靶點。在病毒性肝炎中,僅有B肝病毒為DNA病毒,即包膜、環狀、單鏈、部分雙鏈組成。全球關於HBV領域藥物開發方向,主要集中在B肝病毒生命周期各種步驟、感染持續和相關癌變確切分子機制方向。
黑猩猩是最早被發現,唯一對B肝病毒感染完全敏感的動物,即有免疫宿主。但B肝病毒-宿主範圍較窄,在發現黑猩猩前,發現HBV僅感染人類,相關動物模型研究遇到許多阻力。返回搜狐,查看更多
責任編輯: