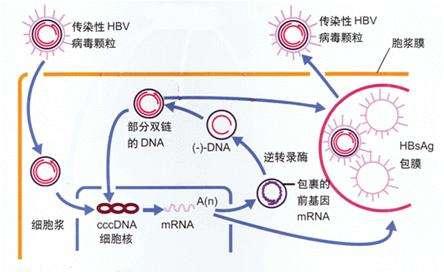
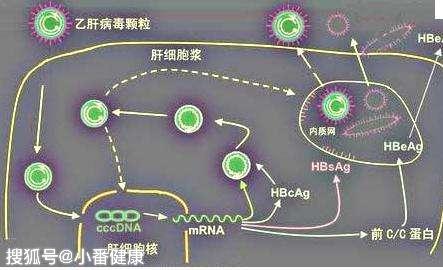
全球B肝藥品市場現狀主要指,儘管已有抗HBV藥物問世,但很少可以完全清除B肝病毒,這就促使科學界積極研究針對HBV更理想藥物。充分了解HBV生命周期對於開發新藥而言,可以導致更合理HBV感染模型與發現開發新候選藥物。

B肝藥物研發早期線索,鋅指蛋白及其衍生物,核酸內切酶應用前景
鋅指蛋白及其衍生物,是全球開發新藥的一種有吸引力方法。鋅指蛋白(ZFP),它是應用在基因組編輯的第一類真核轉錄因子,科學家以往只在3%的人類中發現ZFP。鋅指蛋白核酸酶(ZFN),目前已被廣泛應用在修飾各種細胞基因組之中,包括植物、魚類、小鼠、鴨子以及人類的基因組。而鋅指蛋白的結構域包含三至六個鋅指模塊,每個鋅指模塊,由30個氨基酸所組成。
這些模塊可以包含保守的的Cys2His2鋅指基序,識別DNA主溝中的特定鹼基三聯體。通過工程串聯模塊,可以以高特異性靶向9到18個鹼基對的更長核苷酸序列,還可以修飾鋅指蛋白,用來賦予核酸酶或是轉錄阻遏物的功能。一般而言,這種方法主要是利用DNA結合結構域,融合至單鏈DNA核酸酶之中,將模塊化的鋅指蛋白設計成為鋅指蛋白核酸酶。

內切核酸酶,能夠直接在鋅指蛋白靶向的位點DNA鏈中,造成一個缺口。鋅指蛋白核酸酶被設計成為與相對DNA鏈結合,並且DNA結合結構域一般由5到7個核苷酸的間隔子隔開。所以,當2個鋅指蛋白核酸酶單體,與有義鏈、反義鏈上的相鄰靶位點結合後,就會發生雙鏈DNA切割。因此,科學界以往將特異性識別18至36個鹼基對的鋅指蛋白核酸酶,將其設計成為對目標基因具有唯一性和特異性。
雖然,這種方法的脫靶效應可能較小,但是,鋅指蛋白核酸酶的局限性主要是指模塊DNA結合效率會受到相鄰近的鋅指結構域影響。同理,目前還沒有科學家已經描述出和DNA的64個可能核苷酸三聯體中的每一個結合模塊,這也說明以目前的醫學水準,還無法生成識別任何DNA序列的鋅指蛋白核酸酶。經過科學界長期對這種研究方法的評估,結果發現,TALENs與CRISPR-Cas衍生物並不會受到以上問題的約束。

TALENs,它的中文名稱是轉錄激活因子樣效應物核酸酶,英文全稱是transcription activator-like (TAL) effector nucleases。TALENs是目前基因組編輯核酸酶三大類之一,因此,這些核酸內切酶已經被應用於治療性基因編輯中,並被反覆試驗論證。

當前,全球應用在基因修飾的三種方法是鋅指蛋白核酸酶、轉錄激活因子樣效應物核酸酶和RNA引導CRISPR-Cas系統。因此,鋅指蛋白及其衍生物也是B肝基因療法中基因組和表觀基因組編輯重要方法之一,以小番健康介紹的鋅指蛋白及其衍生物,也在HBV新藥物開發(基於基因新療法)應用中,表現出一定的潛力。返回搜狐,查看更多
責任編輯: