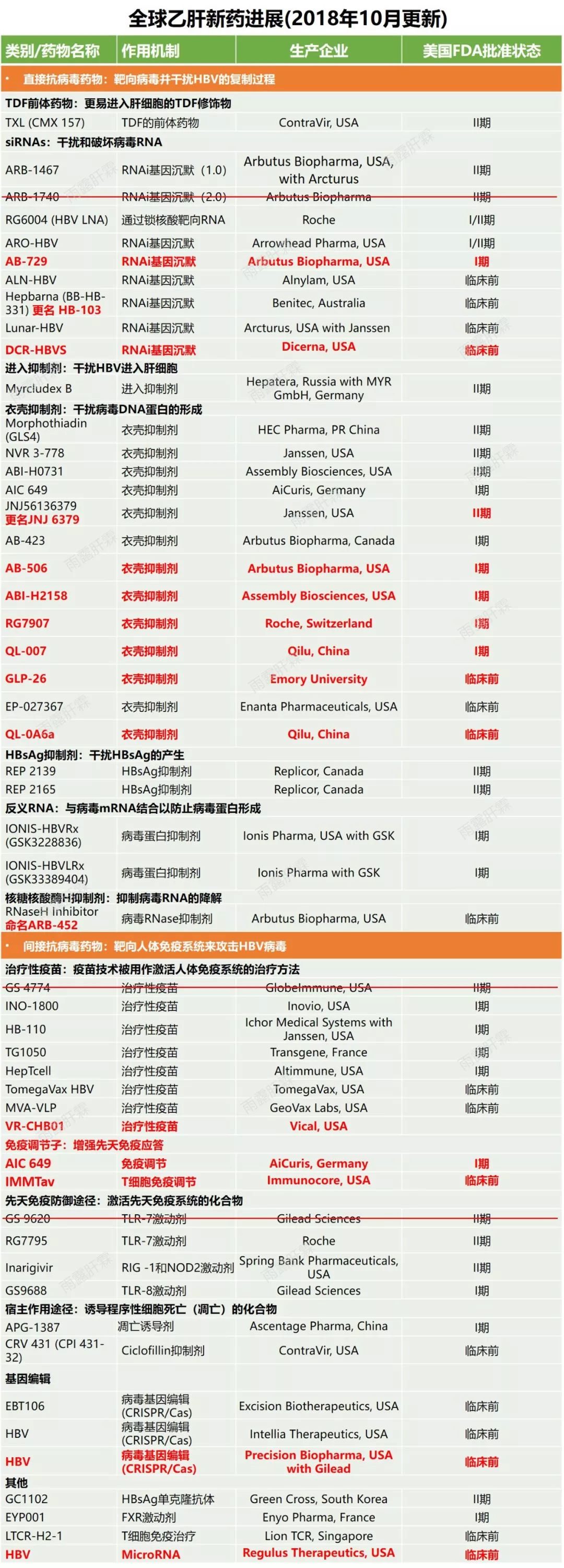
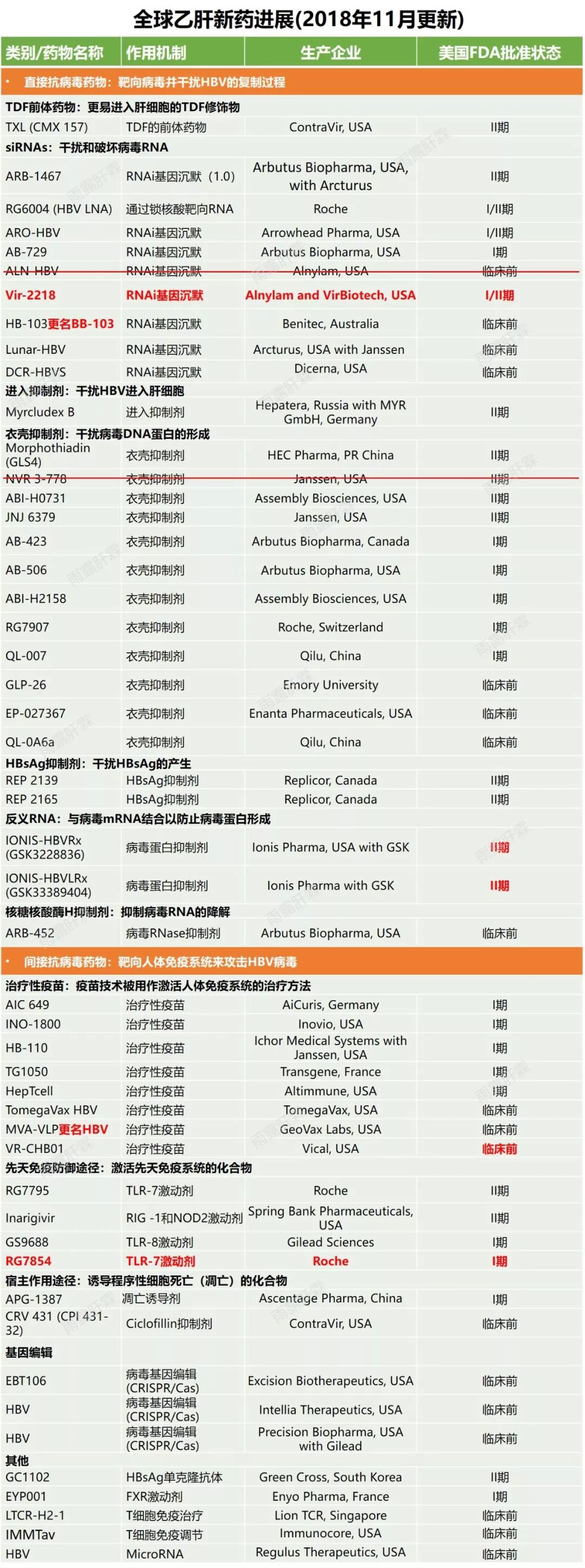
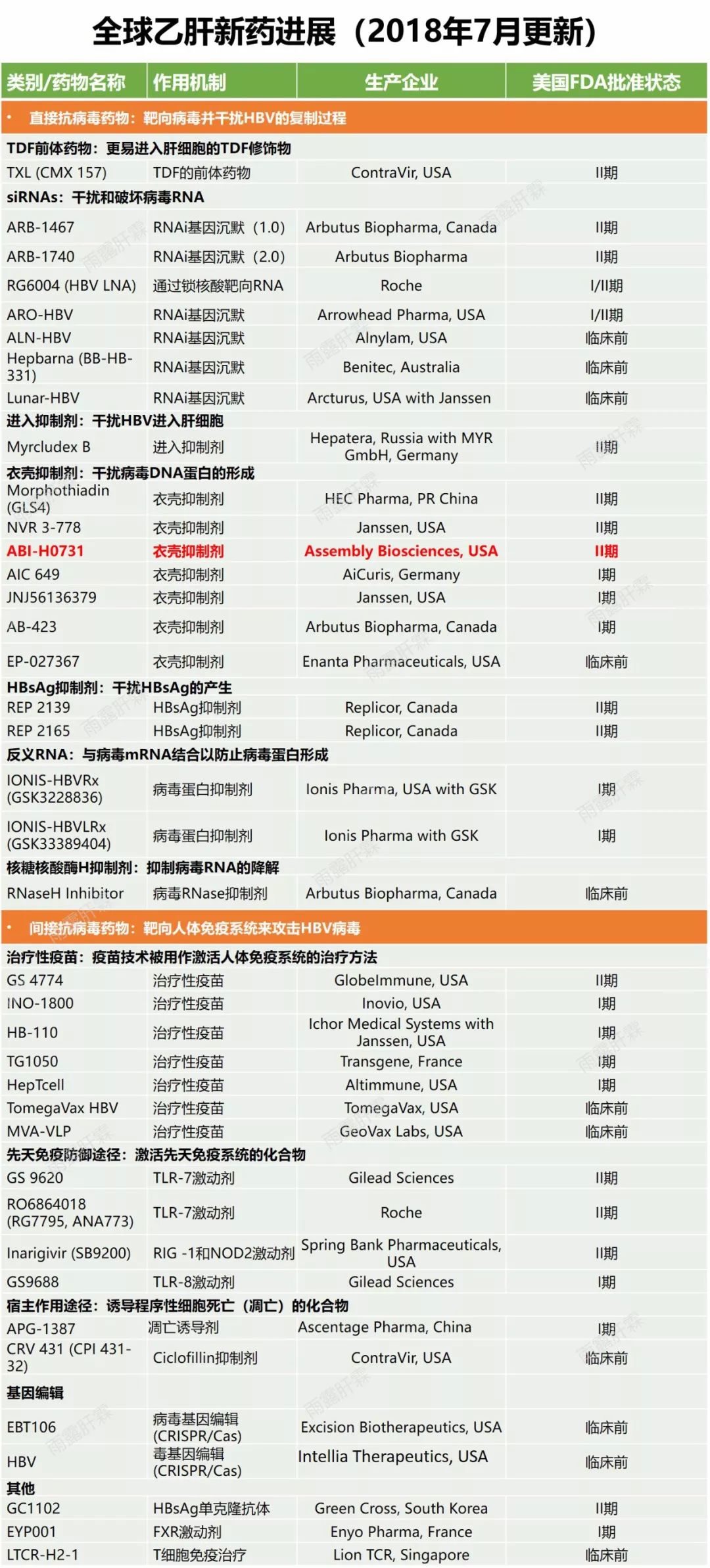
對B肝病毒複製模板共價閉合環狀DNA(cccDNA)具有間接抑製作用的新藥物靶點,其中包含核心蛋白變構調節劑(CpAM)。接下來,我們詳細介紹有關CpAM相關化合物和研究進展。

B肝在研新靶點,核心蛋白變構調節劑CpAM,可間接抑製cccDNA
一、2期因安全性停止開發的ABI-H2158
ABI-H2158是一款由Assembly Biosciences公司科學家研發的第二代HBV-CpAM化合物,去年9月初,該候選藥物在進入2期臨床研究時,觀察到ALT升高和藥物導致的肝髒毒性而終止了進一步臨床開發。
ABI-H2158早在1b期多劑量、多中心遞增隊列14天研究中,在B肝e抗原(HBeAg)陽性、未接受治療的慢B肝受試者中進行。在100毫克、300毫克和500毫克的不同劑量下每日給藥,研究人員觀察到受試者的HBVDNA和pgRNA劑量依賴性下降。使用300毫克劑量後,HBVDNA和pgRNA分別下降2.5 log、2.3 log。但B肝表面抗原(HBsAg)、B肝核心抗原(HBcAg)或HBeAg沒有變化。
在其2期對88名初治受試者進行的一項隨機、多中心、安慰劑對照臨床研究中,受試者按 3:1比例隨機接受300毫克的ABI-H2158+ETV或安慰劑+ETV,持續治療72周。2期安全性評估結果表明,在2名受試者中觀察到了嚴重的3級ALT升高。因無法說明導致肝毒性的其他原因,因此Assembly Biosciences公司與美國FDA溝通後得出結論,導致肝毒性主要原因是ABI-H2158,這款第二代CpAM抑製劑也停止了進一步臨床開發(試驗數據來自:Assembly Bio)。

二、作用機制
相信對核心蛋白(Cp)並不陌生,Cp具有多方面功能,比如容納/包裹HBV基因組。科學家開發CpAMs抑製劑的作用原理是,通過共價連接到二聚體-二聚體界面的疏水口袋來干擾B肝病毒衣殼組裝過程,導致蛋白質四級結構共價修飾。一些全球在研的CpAM還能夠通過在HBV循環的前幾個步驟中分解核衣殼脫殼,導致間接抑製cccDNA作用。
來自:Assembly BioB肝新藥研發管道

三、VBR正在多項2期組合療法
ABI-HO731(vebicorvir,VBR)是一款目前還在研的 II類CpAM。在1期隨機、多中心、安慰劑對照1期研究中,研究人員發現VBR導致HBVDNA和RNA劑量依賴性下降。100毫克、200毫克和300毫克組中,HBVDNA從基線的平均最大下降分別為1.7 log、2.1 log和2.8 log,但B肝表面抗原沒有變化。沒有發生嚴重不良反應,VBR的半衰期長且吸收迅速,其藥代動力學(PK)支持每日給藥。
在VBR進入第2期臨床研究時,研究人員進一步評價了VBR+核苷(酸)類似物(NA)組合療法的抗病毒作用。結果表明,這種組合療法可導致HBVDNA下降更多,HBVDNA下降 5.94 log。而B肝核心抗原、e抗原和B肝表面抗原水準也出現相關下降,分別為1.42 log、1.03 log和 0.86 log(來自:Assembly Bio)。
在另一項組合療法研究中,在停止VBR+NRTIs後,研究人員進一步觀察藥物安全性和病毒學反應。結果表明,在停止VBR單獨使用Nrtl,所有受試者的pgRNA及DNA均立即反彈!(來自2021年美國肝病研究年會)
四、CpAM可分兩類化合物,區分作用機制
小番健康結語:全球有這麽多的在研B肝新藥,它們之中大部分的作用機制和以往已獲批核苷類藥物不同。衣殼抑製劑開發主要是基於對衣殼裝配過程的深刻認識,科學家積極研發相關細分候選藥物,比如衣殼組裝調節劑或核心蛋白變構調節劑,這一大類藥物靶點產生的候選藥物也是最多的。
從原理方面分析,目前最常見的CpAM分為 I類或II類,它們都表現出影響B肝病毒衣殼組裝這個過程。其中,I類化合物是雜芳基二氫嘧啶 (HAP) ,這類化合物能導致衣殼組裝不同步,並形成異常或異常的非衣殼聚合物,從而導致核心蛋白分解。II類化合物包括苯丙烯酰胺 (PPA)和氨磺酰苯甲酰胺 (SBA),它們可以加速組裝過程,讓HBVpgRNA不插入衣殼內,從而導致空衣殼形成。
以上兩大類CpAM都具有潛力,已命名的候選藥物多數都在1期或2期臨床研究中,以II類CpAM化合物進入到臨床研究居多。返回搜狐,查看更多
責任編輯: