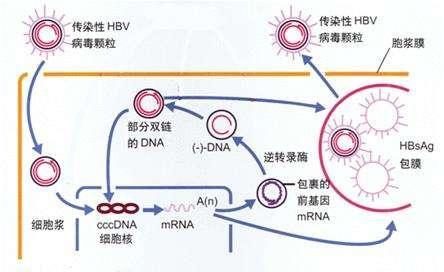
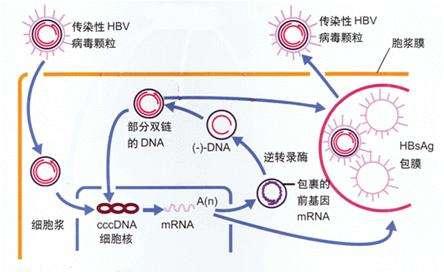
激活人體先天免疫反應的乾預措施,是全球開發B肝潛在新靶點新機制。比如,Toll樣受體激動劑。Toll樣受體(Toll-like receptors,tlr),它已經被藥物學家證明是抵禦微生物入侵的第一道防線,全球有多家藥企基於Toll樣受體激動劑開發新藥當中(下圖:來源吉利德科學新藥研發管線)。

B肝在研新藥GS9620,顯示持久抑製,但cccDNA未下降
該靶點主要通過信號轉導途徑來感知病原體相關的分子模式,從而產生細胞因子。TLR-7和TLR-8激動劑,參與內源性IFN刺激基因的誘導以及JAK/STAT通路等其他信號級聯的激活。吉利德科學的TLR-7激動劑GS-9620,首次在人類肝細胞系HepaRG和感染HBV的原代肝細胞中進行測試時,通過誘導I型IFN,顯示了對B肝病毒複製的持久抑製,但cccDNA水準沒有下降(許多抗HBV藥物同時也為抗HIV藥物)。
而在土撥鼠和黑猩猩動物模型試驗中,研究人員也觀察到類似的結果,但當應用於核苷酸類似物(NA)治療抑製慢性B肝患者時,對B肝表面抗原水準沒有顯著的影響。另一種TLR-7激動劑(RO7020531)和衣殼組裝調節劑RO7049389的聯合治療後,感染重組腺相關病毒(AAV-HBV感染小鼠模型)的小鼠的HBV-DNA和表面抗原水準顯著下降。

這種RO7020531+RO7049389的聯合治療在中國健康志願者中,單次和多次遞增劑量,能夠導致IFN-a誘導的細胞因子產生和ISG的誘導。未來它與其他抗病毒藥物聯合使用的療效仍有待確定。總體上,這種基於免疫療法開發新靶點分支,激活先天免疫反應的乾預措施主要有Toll樣受體激動劑,動物模型證明,單藥對cccDNA和表面抗原沒有影響,但在藥物聯用方面,已觀察到免疫療法分支TLR-7激動劑聯合衣殼組裝調節劑,實現了動物模型時,對HBVDNA及B肝表面抗原明顯調降作用。
另一種免疫療法開發新靶點分支是,維甲酸誘導基因-1(RIG-I)激動劑,其也屬於新型的免疫療法。RIG-I是一種胞漿內PAMP受體,與RNA病毒的雙鏈RNA相互作用。一旦被激活,它可以通過蛋白激酶複合物和NFκB和IRF3轉錄因子的激活,而導致信號轉導,這些轉錄因子又遷移到細胞核,能夠激活ISG,從而產生IFN-a和其他細胞因子,從而啟動抗病毒免疫。

最近在發表在臨床醫學雜誌期刊上,研究人員注意到一些報導稱,pgRNA中存在的epsilon包封信號被RIG-I識別,導致產生III型IFN而不是I型IFN。此外,人們注意到RIG-I抵消了epsilon與B肝病毒聚合酶的相互作用,從而抑製B肝病毒複製。雖然,在研B肝新藥SB 9200已被終止研發,但前期證明它是一種RIG-I/NOD-2激動劑。
在SB 9200研究中,指的是評價其對慢性B肝病毒感染者的安全性、藥代動力學和抗病毒療效研究時,納入了80名未經治療的非肝硬化慢性B肝患者。這些患者被隨機分為12周治療,接受從25毫克到200毫克的遞增劑量的SB 9200或安慰劑,然後再轉為TDF治療12周。負責這些研究人員觀察到,80名e抗原陽性患者(大三陽)和e抗原陰性患者(小三陽)的HBV-DNA和RNA的減少均呈劑量依賴性,而後者更大。
22%的患者在12周或24周時,B肝表面抗原水準下降大於0.5log10。但是,最近SB 9200在進行400毫克劑量與TDF進一步研究時已經被研究人員終止開發。目前看來,基於免疫療法開發B肝新藥難度更高於其他靶點,如衣殼抑製劑、RNAi、B肝表面抗原抑製劑、反義寡核苷酸等等。因此,在新型免疫療法開發研究藥物中,也較其他研究藥物更為頻繁的報導研發終止的報導。

小番健康結語:慢性B肝病毒感染的特點是,由於高水準B肝表面抗原血症而導致的HBV特異性CD8+T細胞喪失或功能衰竭,以及由於B細胞反應不足而無法中和循環中的B肝病毒離子。B肝表面抗原、e抗原以及X蛋白,可干擾感染者固有免疫反應,尤其是信號轉導途徑或其他過程的組成部分,這些過程反過來又會干擾效應細胞(如自然殺傷細胞、T細胞、庫普弗細胞和漿細胞樣樹突狀細胞產生IFN和抗病毒細胞因子 上圖來自本研究人員提供)。
以上試驗數據及最新科研進展,已經發表在臨床醫學雜誌上,歸屬專刊《B肝病毒感染的自然史與臨床後果》(2020年10月1日 Journal of Clinical Medicine)。返回搜狐,查看更多
責任編輯: