12 月 21 日,國家衛健委發布了相關腫瘤診療規範(2018 版),筆者整理了 13 個要點,讓我們全方位學習一下「原發性肺癌」。
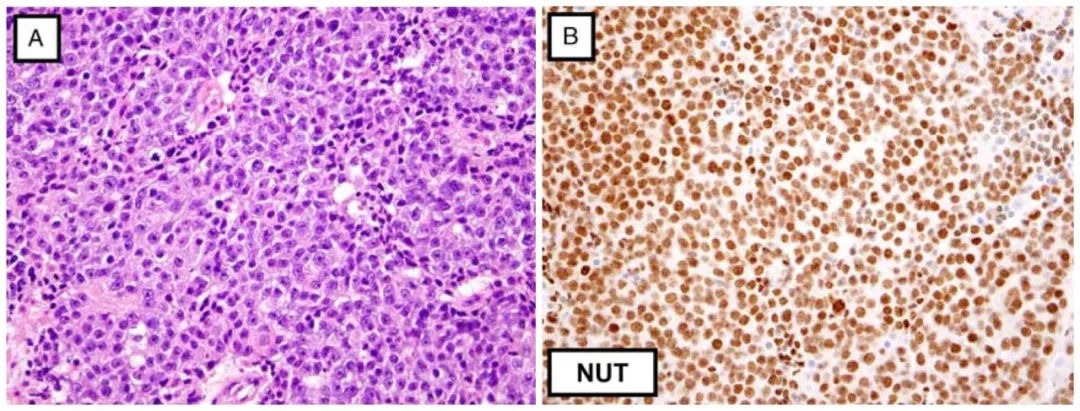
1. 肺癌的分型主要組織類型為鱗狀細胞癌和腺癌,約佔全部原發性肺癌的 80% 左右。
其他少見類型包括:腺鱗癌,大細胞癌、神經內分泌癌、小涎腺來源的癌等。
從病理和治療角度,大致可以分為非小細胞肺癌(NSCLC)和小細胞肺癌(SCLC)兩大類。
2. 危險因素有哪些?吸煙是目前公認的肺癌最重要的危險因素,被動吸煙也是肺癌發生的危險因素,並且主要見於女性。
室內汙染(室內燃料和烹調油煙);
室內氡暴露(建築材料是室內氡的最主要來源,如花崗岩等,);
室外空氣汙染;
職業因素(石棉、石英粉塵等職業接觸);
肺癌家族史和遺傳易感性;
其他因素(營養及膳食等,與肺癌的關聯尚存在爭議)。
3. 肺癌的常見癥狀有哪些?-
原發腫瘤本身局部生長引起的癥狀:咳嗽(最常見),咯血(通常為痰中帶血),呼吸困難,發熱,喘鳴;
原發腫瘤侵犯鄰近器官、結構引起的癥狀:胸腔積液,聲音嘶啞等;
腫瘤遠處轉移引起的癥狀:腦轉移癥狀(頭痛、噁心、嘔吐),骨轉移癥狀(劇烈且不斷進展的疼痛);
肺癌的肺外表現:杵狀指(趾)等。
4. 肺癌常用的腫瘤標誌物
SCLC:NSE 和 ProGRP 是輔助診斷的理想指標;
-
NSCLC: CEA、SCC 和 CYFRA21-1 水準的升高有助於 NSLCL 的診斷。SCC 和 CYFRA21-1 對肺鱗癌有較高的特異性。
注意事項:
① 腫瘤標誌物檢測結果與所使用的檢測方法密切相關,不同檢測方法得到的結果不宜直接比較;
② 不合格標本如溶血、凝血、血量不足等可影響凝血功能、NSE 等腫瘤標誌標誌物甚至肝腎指標等的檢測結果。
③ 標本採集後需儘快送檢到實驗室,標本放置過久可影響 Pro-GRP 等腫瘤標誌物及其他實驗室指標的檢測結果。
5. 影像學檢查的選擇
X 線:對早期肺癌的診斷價值有限,一旦 X 線X光懷疑肺癌應及時行胸部 CT 掃描;
胸部 CT:目前肺癌診斷、分期、療效評價及治療後隨診中最重要和最常用的影像檢查方法;
MRI:對禁忌注射碘對比劑的患者,是觀察縱隔、肺門大血管受侵情況及淋巴結腫大的首選檢查方法;特別適用於判定腦、脊髓有無轉移,腦增強 MRI 應作為肺癌術前常規分期檢查;
-
PET-CT:對於下列情況推薦使用 PET-CT:
a. 孤立肺結節的診斷與鑒別診斷;
b. PET-CT 對於淋巴結轉移和胸腔外轉移(腦轉移除外)有更好的診斷效能;
c. 肺癌放療定位及靶區勾畫;
d. 輔助鑒別常規 CT 無法判斷的腫瘤術後瘢痕與腫瘤複發
e. 輔助鑒別常規 CT 無法判斷的腫瘤放療後纖維化與腫瘤殘存/複發,
f. 輔助評價肺癌療效(尤其是分子靶向治療);
超聲:主要應用於鎖骨上區淋巴結等部位及臟器轉移瘤的觀察;對於胸腔、心包腔積液的檢查及抽液體前的定位;超聲引導下穿刺活檢;
骨掃描:判斷肺癌骨轉移的常規檢查。
6. 肺癌手術適應證
單從肺癌角度考慮,手術的絕對適應證是 T1-3N0-1M0 期的病變;
相對適應證:部分 T4N0-1M0 期的病變;肺癌爭議比較大的手術適應證是 T1-3N2M0 期的病變;
肺癌探索性手術適應證包括部分孤立性轉移的 T1-3N0-1M1 期病變。
手術禁忌證:
肺癌病期超出手術適應證範圍;
全身狀況差,KPS<60 分,結合 ECOG 評分考慮;
6 周之內發生急性心肌梗死;
嚴重的室性心律失常或不能控制的心力衰竭;
心肺功能不能滿足預定手術方式;
75 歲以上頸動脈狹窄大於 50%、75 歲以下頸動脈狹窄大於 70% 以上;
80 歲以上病變需要行全肺切除者;
嚴重的、不能控制的伴隨疾病持續地損害患者的生理和心理功能者伴隨疾病;⑨患者拒絕手術者。
7. 基因檢測的時機、標本、種類
Ⅱ~ⅢA 期 NSCLC、N1/N2 陽性的非鱗癌患者及小標本鱗癌患者:進行 EGFR 突變。
晚期 NSCLC 患者:常規進行腫瘤組織的 EGFR 基因突變、ALK 和 ROS1 融合基因檢測。
有條件者可進行 Braf 突變、C-met 14 號外顯子跳躍突變、Her-2 突變、 Ret 融合基因等檢測和 PD-L1 免疫組化檢測。
不能獲得組織的晚期 NSCLC 患者:可進行血液 EGFR 檢測;
ALK 和 ROS1 融合基因檢測,不推薦首先使用液體活檢標本;
推薦對 EGFR TKIs 耐葯患者進行 EGFR T790M 檢測。
組織學檢測為金標準,在組織不可獲取時,血液 ctDNA EGFR T790M 檢測可作為有效補充。
8. NSCLC 放療的適應證I 期 NSCLC 患者醫學原因不適合手術或拒絕手術,大分割放射治療是有效的根治性治療手段,推薦 SBRT;
術後的 NSCLC 患者,若術後病理切緣陰性而縱隔淋巴結陽性(pN2 期),除了常規接受術後輔助化療外,可加用術後放療,建議採用先化療後序貫放療的順序;
對於切緣陽性的 pN2 期腫瘤,如果患者身體許可,建議採用術後同步放化療。對切緣陽性的患者,放療應當儘早開始;
因身體原因不能接受手術的 Ⅱ~Ⅲ期 NSCLC 患者,如果身體條件許可,應當給予適形放療或調強放療,結合約步化療。
-
對於有廣泛轉移的Ⅳ期 NSCLC 患者,部分可以接受原發灶和轉移灶的放射治療以達到姑息減症的目的。
當患者全身治療獲益明顯時,可以考慮採用 SBRT 技術治療殘存的原發灶和(或)寡轉移灶,爭取獲得潛在根治效果。
9. 小細胞肺癌的放療適應症
-
局限期患者建議初始治療就行同步化放療或先行 2 個周期誘導化療後行同步化放療。
如果患者不能耐受,也可行序貫化放療。
如果病情允許,局限期 SCLC 的放射治療應當儘早開始,可以考慮與第 1 或第 2 個周期化療同步進行。
如果病灶巨大,放射治療導致肺損傷的風險過高,也可考慮在第 3 個周期化療時同步放療;
廣泛期 SCLC 患者,遠處轉移灶經化療控制後加用胸部放療可提高腫瘤控制率,延長生存期。
10. SCLC 預防性腦照射
局限期 SCLC 患者,在胸內病灶經治療達到完全緩解後推薦行預防性腦照射,達到部分緩解的患者也推薦行預防性腦照射;
-
廣泛期 SCLC 在化療有效的情況下,行預防性腦照射亦可降低 SCLC 發生腦轉移的風險。
預防性腦照射推薦時間為所有化放療結束後 3 周左右進行,廣泛期 SCLC 全腦預防照射的決定應當是醫患雙方充分討論,根據每例患者的情況權衡利弊後確定。
11.非小細胞肺癌的圍手術期化療
-
術後輔助化療:完全切除的Ⅱ~Ⅲ期 NSCLC,推薦含鉑雙藥方案術後輔助化療 4 個周期。
輔助化療始於患者術後體力狀況基本恢復正常,一般在術後 4~6 周開始,最晚建議不超過手術後 3 個月;
-
新輔助化療:對可切除的Ⅲ期 NSCLC 可選擇含鉑雙葯,2~3 個周期的術前新輔助化療。
手術一般在化療結束後 2~4 周進行。建議圍手術期化療共進行 4 個周期。
12.肺癌的化療原則
KPS <60 或 ECOG >2 的患者不宜進行化療;
白細胞 <3.0×109/L,中性粒細胞<1.5×109/L、血小板<100×109/L,紅細胞 <2×1012/L、Hb <80 g/L 的患者原則上不宜化療;
肝、腎功能異常,實驗室指標超過正常值的 2 倍,或有嚴重併發症和感染、發熱、出血傾向者不宜化療;
-
在化療中如出現以下情況應當考慮停葯或更換方案:
治療 2 周期後病變進展,或在化療周期的間期中再度惡化者,應當停止原方案;
化療不良反應達 3~4 級,對患者生命有明顯威脅時;出現嚴重的併發症;
除常規應用止吐藥物外,鉑類藥物除卡鉑外需要水化和利尿;化療後每周 2 次檢測血常規;
化療的療效評價參照 WHO 實體瘤療效評價標準或 RECIST 療效評價標準。
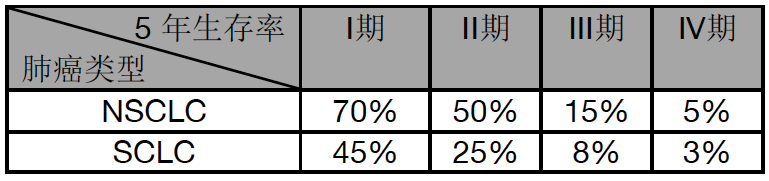
13.肺癌的預後如何?
TNM 分期是預測肺癌患者生存時間的最主要也最穩定的指標。
我國肺癌預後數據:
本文整理自《原發性肺癌診療規範(2018 年版)》