加拿大楊梅生物製藥公司(Arbutus Biopharma)提名兩款新穎作用機制B肝候選藥物AB-101(口服PD-1抑製劑)和AB-161(口服HBVRNA去穩定劑),這兩款B肝在研新藥計劃2022年下半年完成IND支持研究(最快2022年下半年啟動1期研究)。

B肝在研新藥AB-101,AB-161被提名,下半年完成IND支持研究
Arbutus公司目前正有AB-729(RNAi分子)和AB-836(衣殼抑製劑)處於2期組合療法和1期研究中,在楊梅製藥2022年藥物開發計劃更新中,今年將公布AB-729和AB-836多項治療慢性B肝受試者的臨床試驗數據。
即將到來的B肝新藥開發里程碑進展如下:在2022年下半年,將公布三項對慢性B肝(HBV)感染患者使用AB-729正在進行的2a期初步數據,包括:
1、正在進行的AB-729聯合B肝標準療法核苷(酸)類似物(NA)和短期PEG-IFNα-2a治療相結合;
2、AB-729+vebicorvir(“VBR”)+核苷類(NA),一款由Assembly Bio公司開發的在研B肝病毒核心抑製劑(衣殼抑製劑)候選藥物;
3、AB-729+ATI-2173+ Viread®(富馬酸替諾福韋二吡呋酯,TDF),ATI-2173是一款由Antios公司科學家開發的在研專有活性位點聚合酶抑製劑核苷酸(ASPIN)。
另外,將於2022年上半年,啟動一項三聯療法2a期臨床試驗,旨在評價AB-729+VTP-300(Vaccitech公司在研治療性B肝疫苗)+核苷類藥物(NA)。在醫學會議上,展示1a/1b期臨床試驗評價AB-729的多劑量和給藥方案長期治療中和治療後的隨訪數據。2022年上半年公布評價AB-836在慢性HBV患者中的1a/1b期臨床試驗數據。
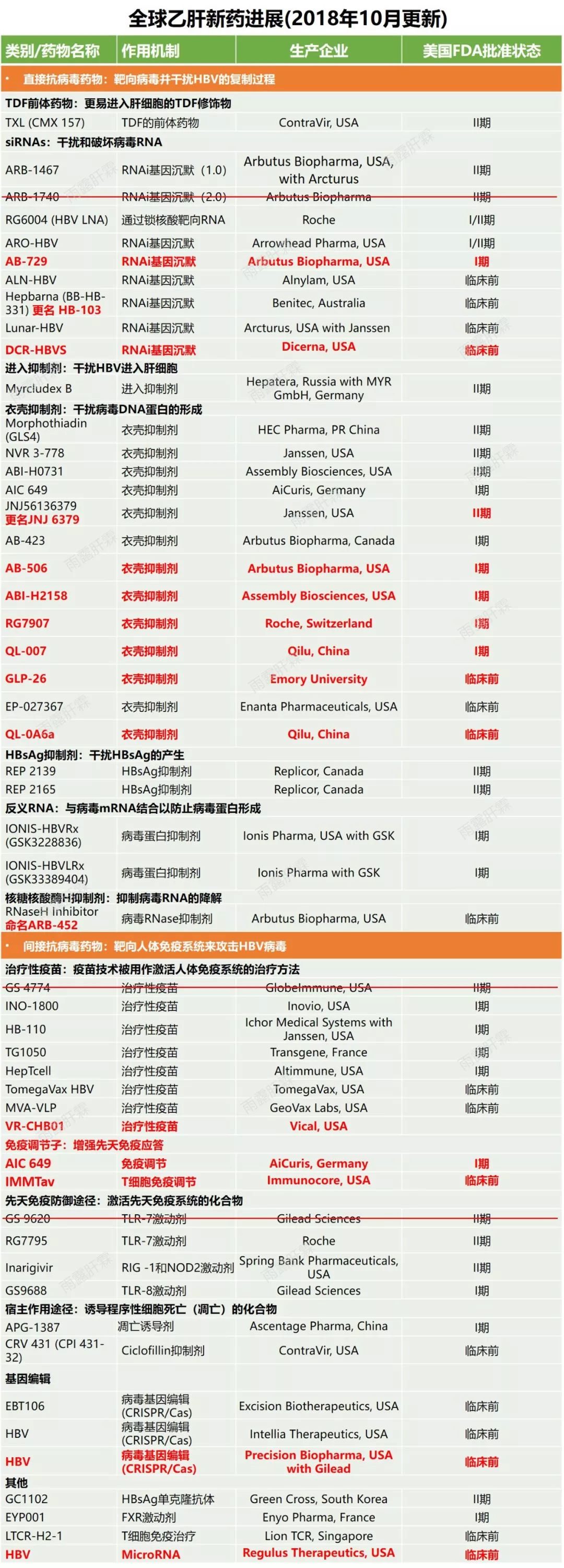
來自:Arbutus Biopharma公司2022年藥物開發計劃,紅色備注為兩款臨床前藥物將完成IND研究

一、提名PD-L1抑製劑和RNA去穩定劑
值得注意的是,楊梅公司還將在2022年下半年,完成兩款最新提名B肝候選藥物的 IND支持研究。包括臨床前口服PD-L1抑製劑AB-101和下一代口服HBV特異性RNA去穩定劑AB-161。
楊梅公司曾開發過一款第一代口服RNA去穩定劑AB-452,452在非臨床研究評估安全性時發現周圍神經病變結果,最後終止了臨床開發。HBV管道中最新分子AB-161已在非臨床研究中,廣泛評估了安全性特徵,這有助於避免發生如AB-452在非臨床研究中暴露的安全性問題。
二、科學家點評
來自Arbutus Biopharma總裁兼首席執行官William Collier點評:基於2021年新藥研發取得的進展,2022年對於HBV患者來說是重要的一年。包括AB-729或AB-836在內的五項臨床試驗正在進行中,目前已準備在2022年全年發布幾項關鍵數據,預計這些數據將支持上述在研新藥進入到 2b期臨床開發。
此外,還打算在2022年通過 IND授權研究來推進口服PD-L1抑製劑化合物AB-101,該化合物旨在重心喚醒慢B肝的免疫系統。同樣,2022年還計劃完成另一款HBVRNA去穩定劑AB-161的IND研究工作。
來自:Arbutus BiopharmaB肝新藥管道,可見紅色備注兩款臨床前藥物AB-101和AB-161已經提名

三、重頭戲在下半年
小番健康結語:從楊梅公司最新B肝新藥管道不難看到,近期最大亮點是兩款即將IND研究的B肝新機制候選藥物AB-101和AB-161。同時,2022年上半年還會啟動一項AB-729+VTP-300+NA的三聯療法2a期臨床試驗,AB-729是一款RNA干擾研究藥物,以往已經公布的試驗數據表明,AB-729能夠大幅調降B肝表面抗原水準,VTP-300是一款在研治療性B肝疫苗,旨在激活或增強慢B肝免疫應答,這項三聯療法通過三種不用作用機理藥物聯合使用來覆蓋HBV生命周期更多步驟,旨在實現功能性治愈HBV。
從楊梅最新B肝管道進展看,2022年下半年將有豐富研究進展,包括公布AB-729三項臨床試驗試驗數據,兩款臨床前藥物完成IND支持研究。返回搜狐,查看更多
責任編輯: