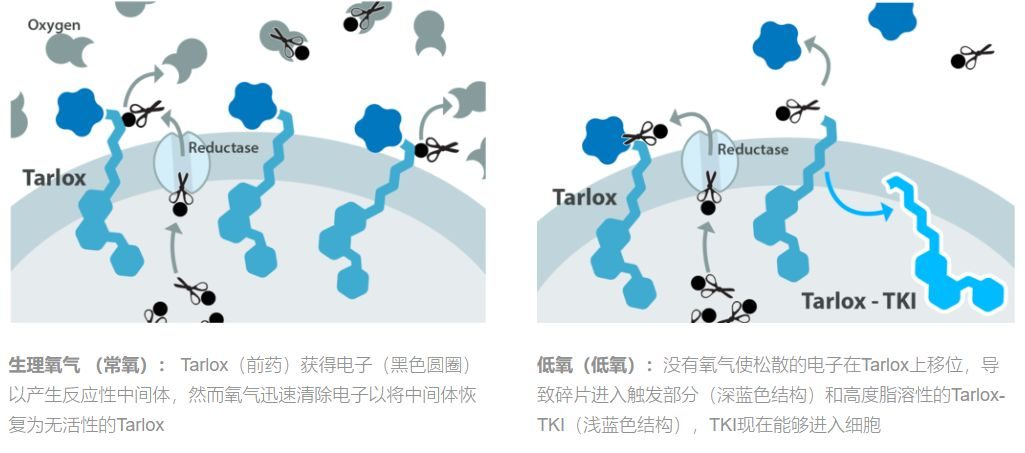
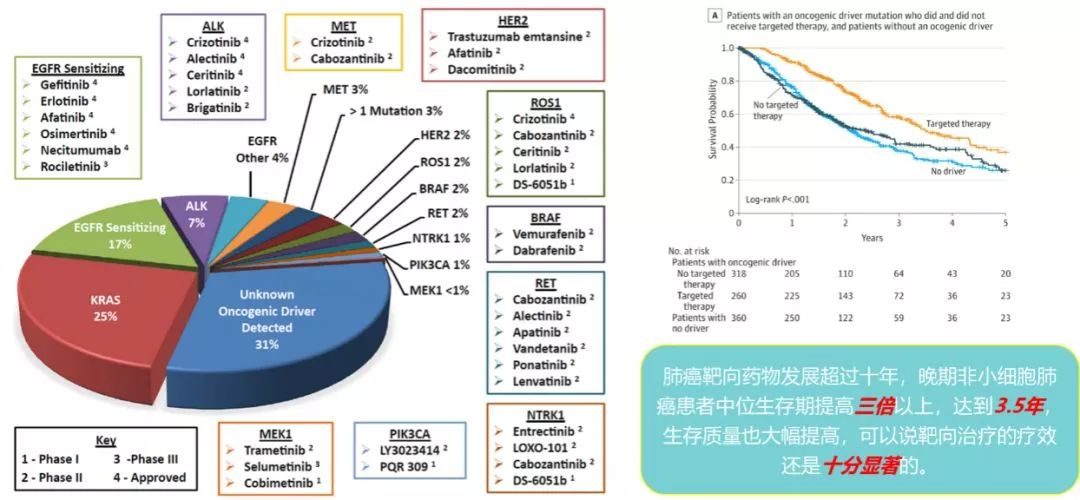
PFS僅2個月!到底為什麼?
晚期EGFR突變型非小細胞肺癌的一線用藥:
EGFR-TKI,
研究數據均支持可獲得較長的無疾病進展時間(PFS)
甚至2-3年的總生存期
但是,為什麼對於這例患者PFS僅2個月?
出乎意料的結果
讓我們一起尋找答案吧~
病史回顧
患者:蔣XX ,男性,46歲。
體檢發現左肺佔位,伴左鎖骨上淋巴結腫大
外院PET-CT:
左鎖骨上淋巴結穿刺病理:腺癌,基因檢測EGFR基因21exon點突變(L858R),ALK(-)
診斷:
左肺腺癌,cT1bN3M0 IIIB期
-
EGFR(+)L858R
PS=0
EGFR-TKI 可延長PFS,
研究數據鼓舞人心
一線治療如何選擇呢?對於晚期突變型非小細胞肺癌,相較於化療,選擇靶向治療可以延長患者的無進展生存期(PFS)和獲得更高的緩解率。以下的八大經典研究均證實針對突變型晚期NSCLC一線TKI,PFS可達8-13月。


靶向治療的EGFR-TKI已經被證實可以大幅改善患者的生存,甚至延長生存期至2-3年。
基於首次淋巴結穿刺檢測結果以及有力的數據支持,對於該患者的一線治療毫無疑問選擇了:EGFR-TKI,埃克替尼治療125 mg tid(2014-6-25)。
一個月後進行複查胸部CT(2014-7-23):左上肺腫塊影,最大層面18×15 mm,淋巴結<1 cm。發現左肺病灶明顯縮小,評估為部分緩解(PR),療效較為滿意,也在意料之中。
但是,1個月後再次複查(2014-8-26)胸部CT,結果卻出乎意料。
意料之外,PFS僅2個月
在本以為療效明顯,歡欣鼓舞之時,2014-8-26再次複查胸部CT發現左肺病灶出現明顯增大,評估為疾病進展(PD)。


考慮患者可能出現EGFR-TKI耐葯,所以選擇了二線治療方案:埃克替尼+DP(多西紫杉醇+順鉑)交替化療,4周期。


經過化療後發現病灶較前出現了明顯的縮小,再次獲得了PR療效。
後續治療也毫無鬆懈,選擇對腫瘤的殘存病灶進行了適形放療(2014-12-22至2015-1-30):左肺病灶、縱膈、雙側鎖骨上淋巴結區6MvXray,DT60Gy/30Fx。同時又進行了2周期的DP方案化療,並繼續使用埃克替尼。
那麼二線治療是否可以成功,
獲得較長的PFS呢?
二線治療基本達到了預期的效果,控制了患者腫瘤約10個月的時間。之後患者再次出現了PD,原發處病灶和鎖骨上淋巴結病灶均較前出現明顯地增大。


此次,二線治療後肺部病灶出現明顯地增大,左側原發病灶及鎖骨上淋巴結均出現增大,化療的療效已經微乎其微,且可以明確得出EGFR-TKI出現了耐葯。
耐葯發生了,下一步應該何去何從?關於耐葯的相關研究很多,一般來說一代EGFR-TKI耐葯機制包括以下兩方面:旁路的激活和EGFR靶點本身的變化,詳細可見下圖:


國內外指南均推薦對耐葯之後可進行再次基因檢測,並且組織優於血液,血液作為有效補充。
那麼對於該患者選擇哪一處病灶進行活檢呢?
一般來說,活檢部位常選擇出現增大的原有病灶(如肺部病灶、轉移的淋巴結)或者新增的轉移灶(顱腦、骨、腎上腺、肝、肺、胸膜、心包、腹膜、皮膚)。再評估技術的可獲得性、安全性,選擇合適的技術。
對於該例患者而言,患者原發灶和轉移灶(左肺和鎖骨上淋巴結)均出現了增大,依據標本的可及性,最終選擇了鎖骨上淋巴結進行二次穿刺活檢,並將血液檢測作為補充。
★ 血漿基因突變檢測結果:


血液基因檢測方面,該患者存在EGFR和HER2的雙突變。
★ 二次淋巴結活檢(2015-6)




淋巴結活檢同樣提示HER2的E20外顯子插入突變。
原發突變or獲得性突變?
由於患者出現耐葯時間僅有兩個月,考慮患者原發突變導致耐葯可能。所以選取了首次組織再次行基因檢測(2014-6),發現在治療前就已有HER2的突變。


根據以上的基因檢測結果可以明確該患者耐葯的機制是因為HER2的E20外顯子突變導致的。所以下一步治療選擇了HER2和EGFR雙重靶點抑製劑:阿法替尼40 mg qd。
治療效果比較明顯,發現原發病灶出現逐步縮小。




尤其到2015年10月左右病灶出現慢慢消散,出現輕微條索影,評估療效為PR。
在患者的治療過程中也採用基因檢測進行了隨訪,2015-11-02再次檢測血漿基因突變情況如下:


結果說明在療效比較好的情況下仍然存在EGFR和HER2的雙突變,此後也仍然選擇了阿法替尼進行後續治療。
總結在關於EGFR-TKI的大部分研究數據均支持可獲得較長PFS的背景下,該例患者卻僅有2個月PFS。結果雖出乎意料,但在臨床醫生診療思維的層層剖析下,原因也逐步浮出水面:HER2與EGFR雙突變是EGFR-TKI短PFS的原因之一。
也有二代測序(NGS)的研究告訴我們,EGFR突變的患者,很多伴有合併突變。而治療後短期耐葯,要考慮多重基因突變的可能,如KRAS、TP53、PIK3CA、HER2。因此,在初始治療之前,採用NGS的方法,全面了解患者的基因突變情況,有可能對患者的治療選擇有更好的判斷。
其次對於二次活檢的標本選擇,建議組織優先,血液補充。在某些基因檢測方面,如EGFR、HER2,血漿和組織標本基因檢測的一致性較高。
此外,驅動基因會隨著治療出現動態改變,具有時間異質性和空間異質性。以該名患者為例,其在後續的治療過程中又出現了一些其他基因的突變,而導致治療方案的轉變。
通過以上病例的剖析、治療的轉變,體現了目前精準治療、個體化治療的精神,對於常規治療無效的腫瘤患者,整合患者的各項臨床信息,找到有效的治療方案。精準治療的發展,得益於腫瘤分子生物學和基因組學的飛速發展,使得腫瘤的治療進入另一鼓舞人心的新時代。
專家點評


張新教授
這是我們5年前診治的一個病例,從這個病例,我們領悟了很多。一些觀念,在幾年前只是推測,但後來被一一證實,以至於現在看起來不稀奇;也有一些問題還需繼續探索。
第一,這個患者EGFR敏感突變,但為什麼埃克替尼治療一度緩解,而PFS卻只有2個月呢?答案是治療前的腫瘤就有EGFR和Her-2兩個驅動基因共突變,當EGFR-TKI抑製了EGFR突變的腫瘤細胞時,攜帶Her-2突變的那群細胞就比較快地成長了起來,表現為腫瘤進展和臨床耐葯。現在越來越多的文獻報導,驅動基因或抑癌基因共突變的肺癌更早耐葯。
第二,從這個病例讓我們也更信服了血漿液體活檢的價值。這個患者首次組織病理診斷時,按那時的常規隻做了EGFR和ALK突變檢測,並沒有做更多的基因檢測,直到發生EGFR-TKI耐葯後做血漿液體活檢,才檢測出Her-2突變,我們回過頭來檢測最早的組織標本,才發現Her-2早就存在。實際上該患者在阿法替尼耐葯後,液體活檢還發現了更複雜突變的動態變化。
第三,這個病例還讓我們思考更多靶向治療相關問題:EGFR與Her-2共突變的腫瘤,到底是有兩群細胞各含一個驅動基因呢、還是每個細胞都含有兩個驅動基因?Her-2作為肺癌少見驅動基因,阿法替尼等Her-2抑製劑為什麼療效遠不如EGFR、ALK等相應的TKI呢?是不是Her-2更多地與某些基因共突變呢?
互動有禮
請趕緊在「留言區」寫下你今天的
學習心得!!!
截止明天中午12:00
點贊數最高的網友將有機會獲得
呼吸專業相關書籍一本!
想參與更多病例討論?
歡迎加入醫學界-中山呼吸半月談討論群,
ps:驗證消息「醫院-姓名」,便於入群審核~
專家簡介


張新教授
主任醫師,醫學博士,復旦大學附屬中山醫院呼吸科副主任,肺部腫瘤與呼吸介入科主任,中華醫學會呼吸分會介入學組委員,中國醫藥教育協會肺部腫瘤專委會常委,亞太醫學生物免疫學會常務理事,上海市抗癌協會呼吸腫瘤介入專委會副主任委員,上海市抗癌協會肺癌分子靶向與免疫治療專委員會副主任委員,《上海醫藥》雜誌編委。
從事呼吸及肺癌診療工作27年,先後從事的研究工作有肺癌基因診斷及基因治療、靶向與化療的聯合應用、肺癌液體活檢、磁導航引導肺活檢等,作為分中心PI參加多項國際臨床試驗。參編《實用內科學》等專著6部,發表論文三十餘篇。


張勇
復旦大學附屬中山醫院呼吸科副主任醫師,博士
中國醫師協會呼吸分會研究工作工作組委員
中國醫師協會內鏡分會呼吸內鏡青年委員會委員
中國醫藥生物技術協會基因檢測技術分會委員
如何下載醫生站?
按住圖中二維碼3秒鐘,識別二維碼後,按提示步驟下載並安裝。
TAG: |