急性心肌梗死(AMI)是嚴重的心血管急症,心源性休克(CS)是AMI最危重的併發症之一。在第十二屆東方心臟病學會議(OCC 2018)上,貴州醫科大學附屬醫院李偉教授詳細講解了如何處理合併心源性休克的AMI。
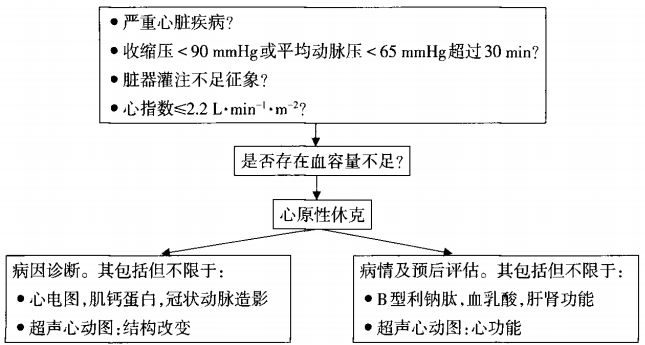
心源性休克的定義及診斷標準心源性休克是指由於心臟本身病變導致心輸出量顯著減少,周圍循環衰竭,廣泛的組織缺血、 缺氧和重要生命器官功能受損而產生的一系列臨床徵候。AMI是心源性休克最常見的原因。
休克診斷:平時高血壓者收縮壓持續<90 mmHg(平時血壓正常者收縮壓<80 mmHg),或平均動脈壓較基礎值下降30%,患者往往伴有心率加快。臨床表現為四肢濕冷、脈搏細弱、尿量減少(<20~30 ml/h),嚴重者神志改變。
心源性休克的診斷:①休克+外周臟器低灌注表現;②存在心源性疾病導致心輸出量下降;③除外低血容量、過敏性、創傷性、感染性、中樞性原因。
血流動力學診斷標準:①無循環支持時,心臟指數(CI)<1.8 L/min/m2,或者有輔助循環支持時,CI<2.0~2.2 L/min/m2,代表心輸出量下降;②PCWP在18~20 mmHg時,開始出現肺淤血;>40 mmHg時,為肺水腫。
心源性休克的處理建議表1 2017年ESC STEMI指南心源性休克管理建議
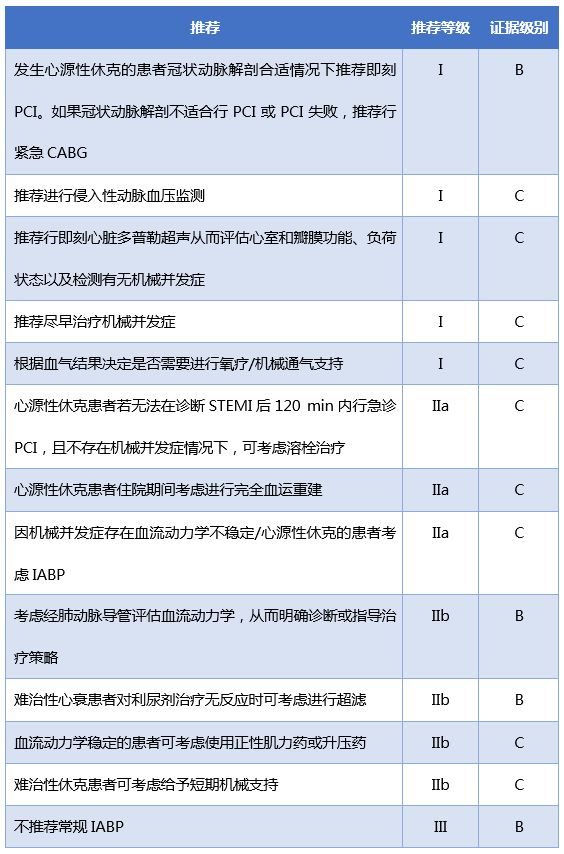

表2 2015年ESC NSTE-ACS指南心源性休克管理建議
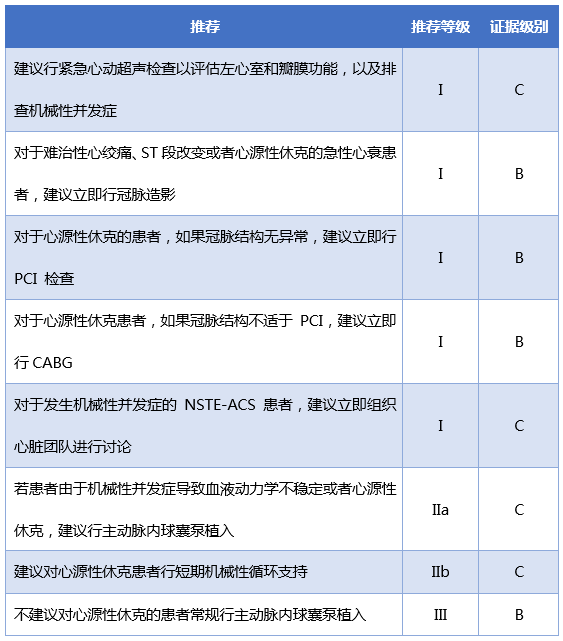

表3 2015年ESC NSTE-ACS指南對侵入性冠脈造影和血運重建的推薦


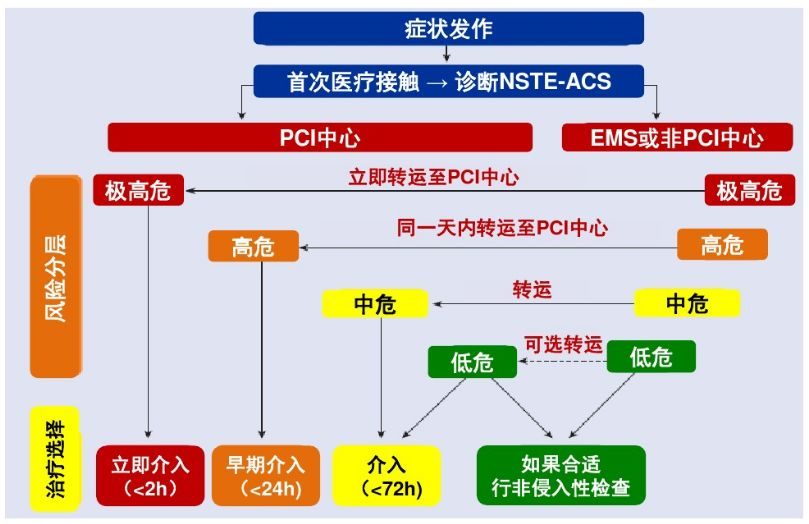

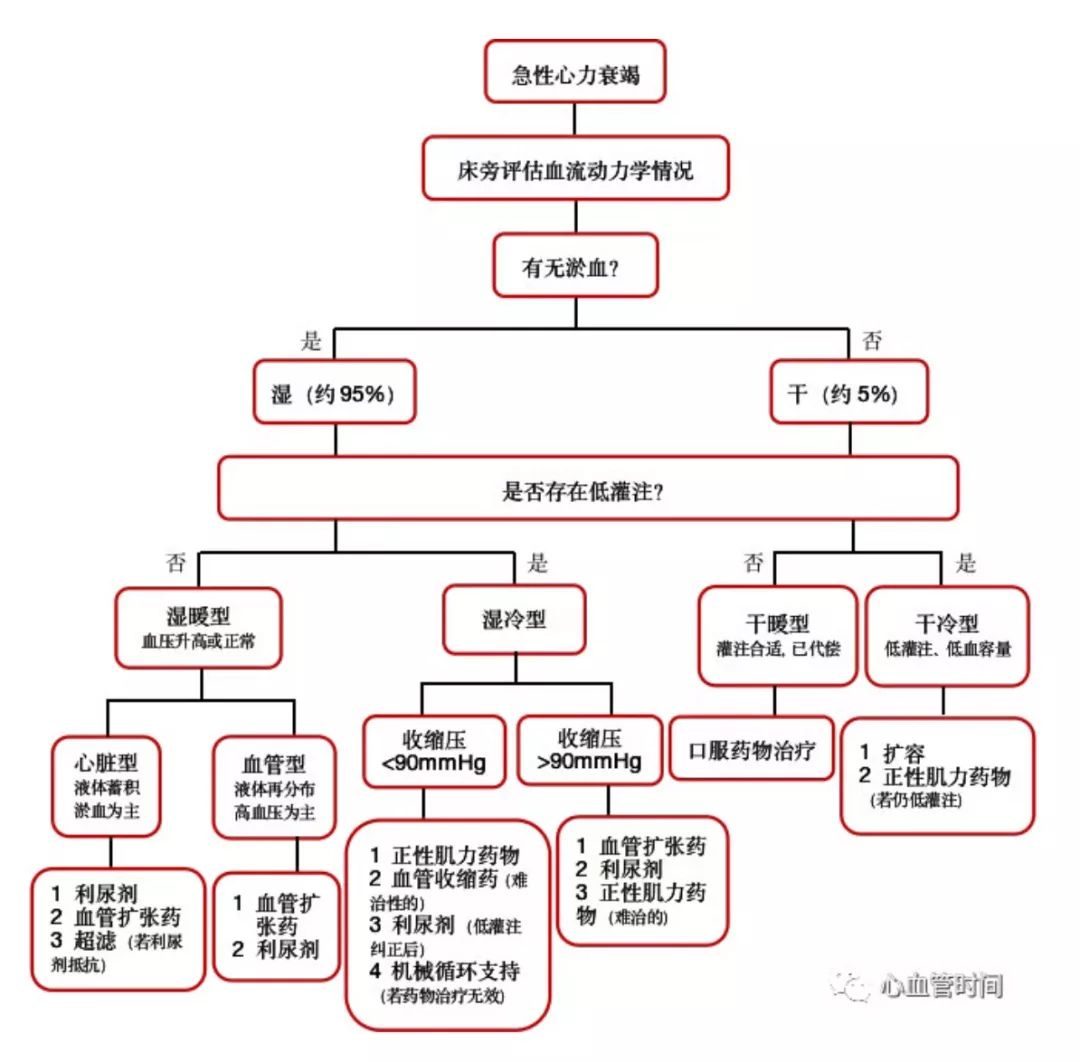
圖1 2015年ESC NSTE-ACS指南心源性休克處理流程
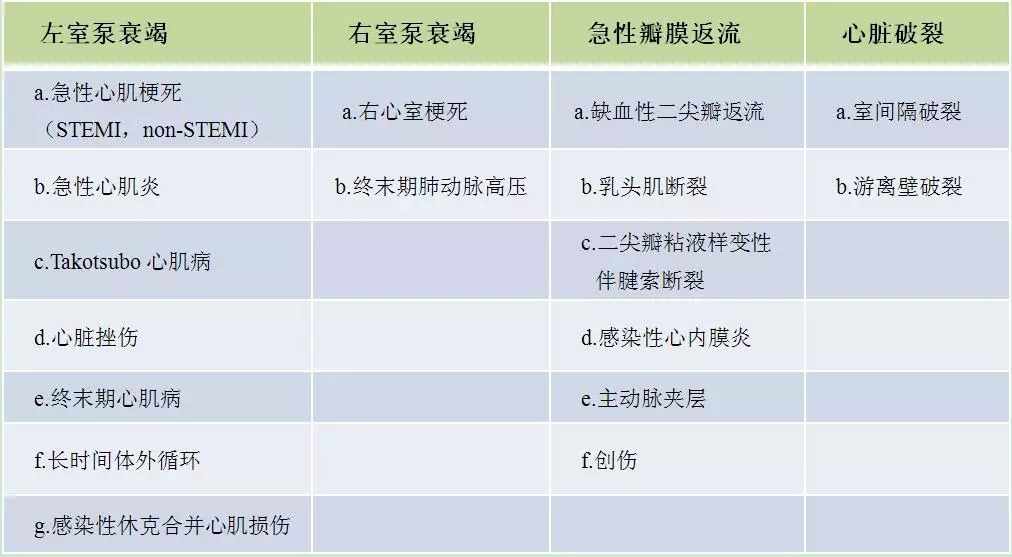
AMI合併心源性休克的類型及處理1. AMI後左心急性泵衰竭合併心源性休克、肺水腫
?收縮壓<80 mmHg,皮膚濕冷、少尿等低灌注表現
?PCWP>20 mmHg,呼吸窘迫、氧飽和度下降、X光呈肺淤血
?處理:強心、利尿改善左心功能、IABP等心臟支持裝置改善灌注
2. AMI後右心泵衰竭合併心源性休克
?以低血壓、低灌注表現為主
?SBP<80~90 mmHg,尿少、皮膚濕冷
?PCWP<20 mmHg,X光不表現肺淤血,尚能平臥
?處理:補液,對正性肌力藥物反應差
3. 非低血壓心源性休克
?呈高交感活性狀態,往往是第一類型經過處理後的表現。
?收縮壓>90 mmHg,但仍表現為低灌注、外周阻力升高、四肢濕冷、脈搏細弱、心率快、尿少,死亡率接近50%
?處理:可嘗試用擴血管和血管活性藥物、IABP等心臟支持裝置可能有益
4. 低血壓為主要表現
?外周灌注尚可,相對多見,且為良性
?收縮壓<90 mmHg,尿量輕度減少,肺部無濕囉音,X光無肺淤血,為隱性泵衰竭
?處理:避免過度補液、利尿,對正性肌力藥物反應好
5. 右室心肌梗死合併心源性休克
?及時識別右室心肌梗死導致的心源性休克:在18導聯心電圖中,V3R、V4R導聯ST段抬高,III導聯ST段較II導聯高
?單純下壁心肌梗死合併低血壓,應想到右室心肌梗死
?在無肺淤血(肺部無囉音/X光無肺淤血)情況下,頸靜脈充盈,應想到右室心肌梗死
?處理:及時開通血管;嚴重時快速補液,保證右心室前負荷,避免擴血管藥物、β受體阻滯劑、利尿劑;易合併緩慢性心律失常,應及時糾正,必要時可用臨時起搏器;糾正房顫
6. AMI合併心源性休克的總體處理原則
?病因治療:血運重建、抗血小板、抗凝、調脂穩定斑塊
?處理誘因和加重因素:血容量、血氣、電解質、血氧、鎮痛,及時調整降壓藥物
?維持血流動力學穩定和臟器灌註:血管活性藥物、IABP等心臟支持裝置
(1)血管活性藥物:兒茶酚胺類藥物
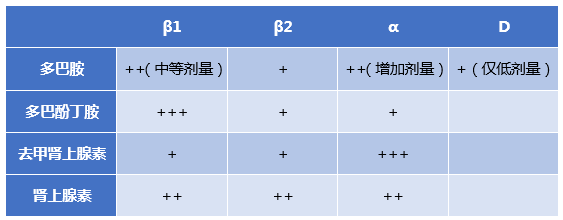
表4 兒茶酚胺類藥物的作用靶點

(2)IABP使用
血管活性藥物不能改善臨床狀況時,如心率快、四肢末梢濕冷、少尿、心衰發作,或者出現機械併發症,如乳頭肌斷裂、室間隔穿孔、遊離壁破裂等,可以使用IABP。需除外主動脈瓣關閉不全。
IABP增加舒張期冠脈血流,減輕心臟後負荷,有效逆轉阻滯低灌注,減少心肌耗氧。IABP應用越早越好,獲益為:預見性>補救性。
(3)Impella、Tandem Heart
能夠更好地降低左室負荷,血流動力學支持效果更佳。在改善CI及臨床獲益方面優於IABP,更適合嚴重心源性休克。但是,出血併發症多、花費高、操作複雜。
(4)ECMO
ECMO能提供有效的心肺雙重功能支持,能為PCI及CABG提供更好的過渡和支持,能降低AMI合併心源性休克患者的死亡率。需要注意的是,截肢、卒中、出血及再生術等相關併發症發生率較高。