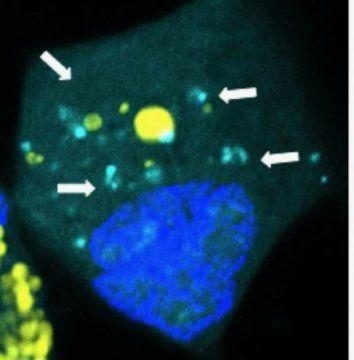

在一項「概念證明」研究中,約翰霍普金斯大學醫學院的科學家表示,他們已經成功地提供了納米級的遺傳密碼包,稱為microRNA,用於治療植入小鼠的人腦腫瘤。超小容器的內容被設計成針對癌症乾細胞,這是一種產生無數後代的細胞「種子」,是消除大腦惡性細胞的無情障礙。
「腦癌是其遺傳構成方面最廣為人知的癌症之一,但我們尚未開發出良好的治療方法,」神經病學,腫瘤學和神經科學教授John Laterra博士說。約翰霍普金斯大學醫學院和肯尼迪克裡格研究所的研究科學家。「癌症乾細胞的復原力和血腦屏障是主要的障礙。」
進入大腦的血液通過一系列作為保護屏障的血管過濾。但是,這種血腦屏障通過靶向癌症乾細胞來阻斷有可能徹底改變腦癌治療的分子藥物,Laterra說。
「為了使腦腫瘤治療現代化,我們需要繞過血腦屏障的工具和方法,」生物醫學工程,眼科,腫瘤學,神經外科,材料科學與工程以及化學和生物分子工程教授Jordan Green博士說。在約翰霍普金斯大學醫學院。「我們需要技術來安全有效地將敏感的基因藥物直接輸送到腫瘤而不會破壞正常組織。」
格林說,一個典型的例子就是膠質母細胞瘤,即亞利桑那州參議員約翰麥凱恩正在與之抗爭的腦癌形式,這往往需要反覆手術。拉特拉說,醫生可以清除他們可以看到的腦腫瘤組織,但惡性腫瘤通常會迅速恢復。大多數膠質母細胞瘤患者在確診後不到兩年。
科學家長期以來一直懷疑癌症乾細胞是導致膠質母細胞瘤和其他癌症複發和傳播的根源。這些乾細胞會產生其他癌細胞,如果它們躲避外科醫生的刀,就會導致一種全新的腫瘤。
作為約翰霍普金斯Kimmel癌症中心成員的Laterra和Green設計了一種方法,可以有效地將超微小的microRNA包裝到已建立的腦腫瘤中。microRNA靶向腦癌乾細胞,以阻止其傳播和維持腫瘤生長的能力。
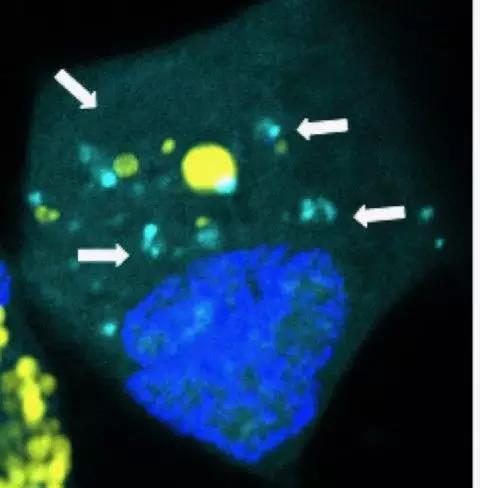
包裝由可生物降解的塑料製成,類似於用於手術縫合的材料並且隨著時間的推移而降解。它們比人類頭髮的寬度小1000倍,並且通常是細胞用來交流的天然成分的大小和形狀。當癌細胞吞噬數據包時,它們會分裂並釋放其microRNA「有效負載」,特別是microRNA需要在癌細胞內起作用的地方。
納米包裝中包含特異性結合與兩個基因連接的信使RNA的微小RNA:HMGA1和DNMT,它們共同起作用以調節細胞中的基因表達程式。
當microRNA與這些信使RNA結合時,它們會阻斷它們的蛋白質製造能力,並關閉驅動癌細胞乾細胞特徵的程式。如果沒有它們的乾細胞特性,癌細胞就會更加分化,它們會失去傳播腫瘤的能力,而且它們可能更容易受到輻射和藥物的影響。
在他們的實驗中,約翰霍普金斯大學的科學家將人類膠質母細胞瘤細胞植入18隻小鼠體內。為了模擬治療現有腫瘤的臨床挑戰,科學家們等待45天才對動物進行治療,以確保它們具有良好的腫瘤形態。一半的動物接受含有活性microRNA的納米包裝直接輸注到他們的腦腫瘤中,另一半接受含有非活性microRNA的納米包裝。為了分離納米粒子的影響,科學家們使用了沒有免疫系統T細胞的小鼠,這些小鼠靶向癌細胞。
接受無活性microRNA(對照)的9隻小鼠中有5只在兩個月內死亡,其餘對照小鼠在90天內死亡。接受活性microRNA的9隻小鼠中有3隻持續長達80天,其中6隻活到133天。對這六種人進行人道安樂死,檢查分離的小鼠腦是否存在腫瘤。
所有對照小鼠在死亡時腦中都有大腫瘤。接受活性microRNAs並且活到133天的四隻小鼠沒有腫瘤,兩隻小的小鼠。
格林說,許多基因藥物都是針對一個基因而設計的。約翰霍普金斯團隊在本研究中使用的納米粒子類型可以封裝多種類型的microRNA來靶向多個基因網路。
Laterra說,當腦癌乾細胞內化納米顆粒並轉變為非乾細胞狀態時,臨床醫生可以利用這種情況,並提供輻射或其他藥物來殺死現在脆弱的細胞。
格林說,其他地方的科學團隊正在使用基於脂質的材料開發microRNA包,並且一些標準的化學療法是在稱為脂質體的脂肪納米顆粒中提供的。
Green和Laterra說,他們研究中的納米粒子能夠滲透整個腫瘤,因為嚙齒動物的大腦很小。人腦較大,可能需要泵和導管來彙集大腦中的納米顆粒。
約翰霍普金斯大學的團隊正在努力擴大其納米粒子的開發,並在申請許可開始對人進行臨床試驗之前標準化其穩定性和品質。
該研究小組已就該研究中使用的部分技術申請了專利。
TAG: |