醫藥研發技術和新藥研究息息相關,新的設計酶CRISPR/Cas9 RNA引導的核酸酶系統引起了科學家的興趣,這是一種提供直接攻擊B肝病毒基因組的先進技術,我們就來談談B肝病毒和CRISPR/Cas9近幾年所遇到的一些技術路徑問題和潛力。

B肝設計酶,未來開發前景,應識別各種HBV及最小脫靶效應
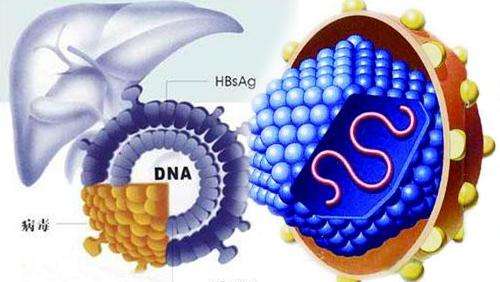
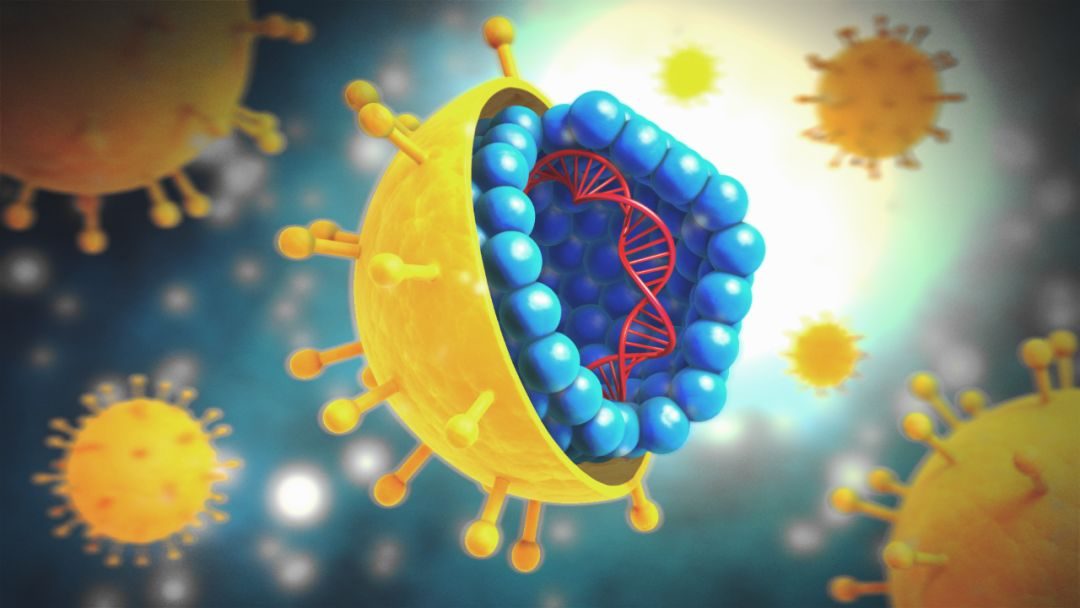
B肝病毒(HBV),是嗜肝病毒科的成員之一,嗜肝病毒科是具有松弛環狀DNA(rcDNA)基因組的小型非細胞病變病毒家族。當感染後,rcDNA基因組在感染細胞的細胞核中,轉化成為了共價閉合環狀DNA(cccDNA)。B肝病毒把人類當成了其唯一的天然宿主,幾乎隻感染肝細胞。
HBV基因組,包含4個重疊的開放閱讀框(ORF),它們通過使用替代起始密碼子編碼7種病毒蛋白。HBV X(HBx),它是HBV編碼蛋白之中最小的,存在所有的哺乳動物嗜肝病毒當中。HBx通常被認為是一種非結構蛋白,而且已經被科學家證明,在HBV生命周期、病毒-細胞相互作用以及HBV相關的HCC中發揮著多種功能意義!

難點:當我們了解HBV主要結構以後,以現有抗病毒藥物還無法治愈HBV感染。因為要想成功根除HBV,則需要滅活病毒基因組,該基因組主要以遊離共價閉合環狀DNA(cccDNA)形式,存在於宿主細胞之中,在較小程度上,會以染色體整合序列的形式存在。
尚待解決問題:對設計核酸酶的未來開發應用前景,必須能夠識別各種B肝病毒基因型,並且可以導致最小的脫靶效應才行。包膜HBV的基因組,包含一個環狀、部分雙鏈DNA,它是使用逆轉錄酶從RNA中間體合成。目前為止,科學家已經發現了HBV基因組中,有8種主要基因型(A至H),在HBV感染細胞中,病毒遺傳信息,就是人們熟知的以cccDNA(共價閉合環狀DNA)形式存在附加體中,在人類基因組中以整合DNA形式存在著,上面也有提到。

而且這種病毒庫還特別持久,讓HBV治療變得相當困難。現有主要有兩種被科學家認可的方法,即干擾素-α和核苷(酸)類似物。干擾素-α,主要有價格昂貴,可能會導致嚴重不良反應等;核苷(酸)類似物通常需要長期甚至終身給藥,並且可能會發生基因逃逸突變。
多數核苷(酸)類似物可以接近病毒抑製,但還不能從體內完全地消除HBV,這主要是因為B肝病毒DNA也是肝細胞DNA的一個組成部分。藥物研發人員要想開發設計出,完全治愈HBV感染,就必須根除或至少大量減少受到感染肝細胞中的cccDNA。

小番健康結語:到目前為止,隻關注到,要想實現大量減少感染肝細胞中cccDNA的方法,可能會和其他在研新藥物結合使用,比如免疫調節劑、小分子抗病毒抑製劑、RNAi等等。科學家在過去幾年中,已經至少開發了三種新技術,比如鋅指核酸酶 (ZFN)、轉錄激活因子樣效應核酸酶 (TALEN)和最近人們熱議的CRISPR/Cas9 RNA引導的核酸酶系統。
潛力:實際上,科學家已經在不同的測試系統中,通過使用ZFNs、TALENs和CRISPR/Cas9,實現了對HBV的直接抗病毒作用。但是,正如最近小番健康介紹的,這些新技術還有一些技術路徑問題沒有解決,除了核酸酶的最佳傳遞與循環HBV毒株中最理想靶位點保護,以及潛在的脫靶效應的高度相關問題。
這是一種好的潛在直接靶向cccDNA方法,但科研人員還要解決上述問題,才可能實現藥物從臨床前進入臨床研究。返回搜狐,查看更多
責任編輯: