葯明康德/報導
圖片來源:123RF
藥物研究
研究藥物:丙氨酸布立尼布片(其他命名:ZL-2301,Brivanib alaninate),由再鼎醫藥(Zai Lab)申報臨床開發的抗癌靶向葯——口服雙重靶點激酶抑製劑,針對VEGFR和FGFR的選擇性雙重抑製劑。
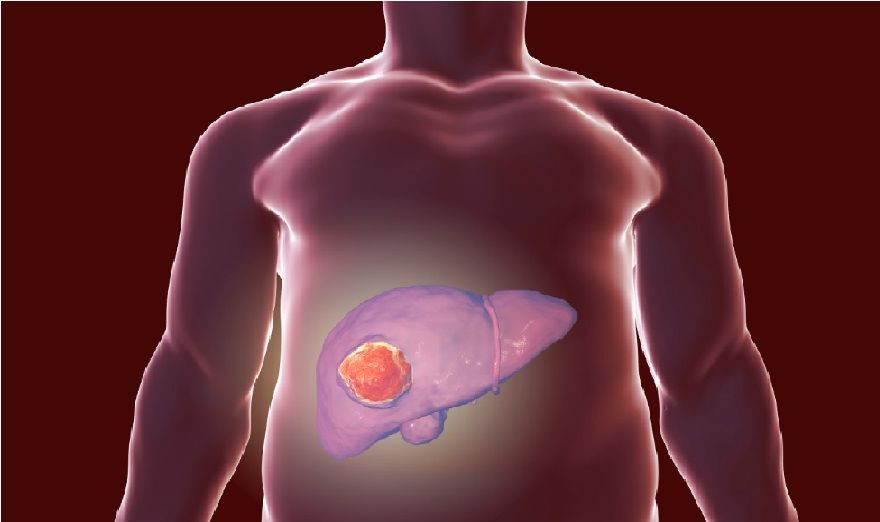
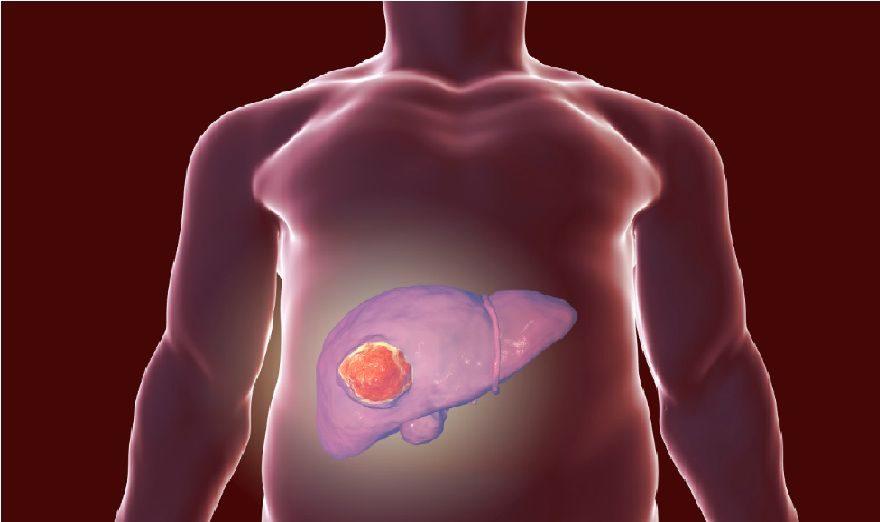
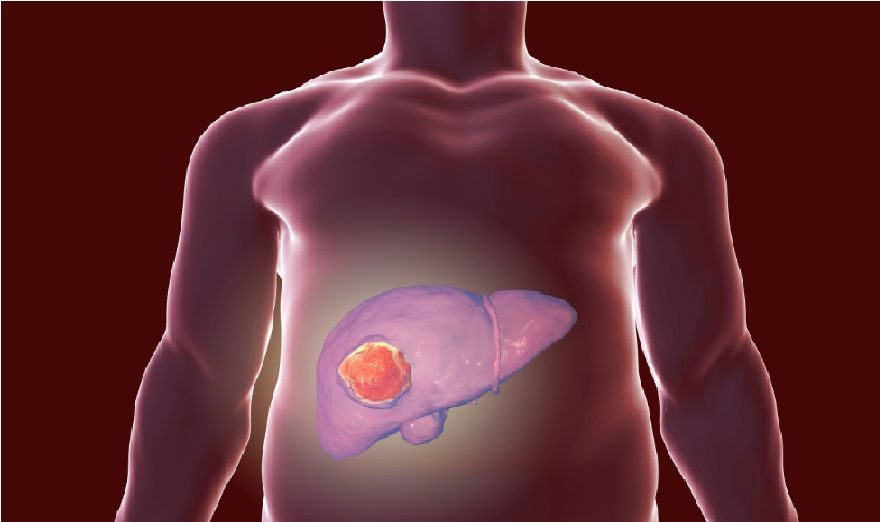
研究適應症:晚期肝細胞癌(HCC)。
首次公示:2018-06-07
研究標題:在既往經過治療晚期肝細胞癌患者中評價丙氨酸布立尼布有效性安全性的隨機雙盲平行對照III期研究。
研究目的:評價丙氨酸布立尼布加最佳支持治療(BSC)對比安慰劑加最佳支持治療(BSC)治療晚期HCC患者的有效性和安全性。
研究範圍:本研究為國內試驗,本次招募計劃,面向中國患者,目標入組人數:中國348人。臨床參加機構(醫院),參見文末列表。
主要入選標準:
1.確診為晚期肝細胞癌的患者,年齡18-75歲;
2.巴塞隆納肝癌臨床分期(BCLC)C期或B期;
3.肝功能狀態Child-Pugh A級或評分≤7分的B級;
4.不適合接受局部治療或局部治療(手術或放療等)失敗;
5. 既往接受過一種系統化療和/或一種分子靶向藥物治療失敗或不耐受;
6.體能狀態ECOG評分0或1分;預期生存≥12周。
(詳細說明見下文列表,最終入選標準由醫生評估)
本次臨床招募和實施方案,已經在中國國家食品藥品監督管理總局登記註冊(註冊號:CTR20180831)。按照方案規定,入選患者將接受:
丙氨酸布立尼布+最佳支持治療(研究組),或
安慰劑+最佳支持治療(對照組)
考慮參與或有興趣了解有關研究資訊,請訪問文末聲明網址鏈接,獲得更多詳情。符合所有合格性條件(包括入選和排除標準)的患者,在參與臨床研究過程中,將可獲得免費的研究相關檢查和治療。顧問方式,參見文末的研究人員和醫療機構(醫院),了解實時動態更新資訊。
本次臨床招募的入選標準包括:
| 1 | 自願簽署知情同意書; |
| 2 | 18-75歲,性別不限 |
| 3 | 經病理組織/細胞學或臨床診斷確診的晚期HCC患者 |
| 4 | 巴塞隆納肝癌臨床分期(BCLC)C期或B期,不適合接受局部治療或局部治療失敗 |
| 5 | 根據RECIST v1.1標準證實具有至少有一個可測量病灶。位於既往放療照射野內或局部治療區域內的靶病灶如果證實發生疾病進展,則認為其為可測量病灶 |
| 6 | 有明確病歷或證據記錄既往接受過一種系統化療(單葯或聯合用藥的全身化療)和/或一種分子靶向藥物治療失敗或不耐受的晚期HCC患者 |
| 7 | 前一次抗腫瘤治療結束距開始本研究用藥≥2周,且既往治療相關不良事件恢復至NCI CTC AE≤1級 |
| 8 | 肝功能狀態Child-Pugh A級或評分≤7分的B級 |
| 9 | ECOG體力狀態評分為0或1 |
| 10 | 預期生存時間≥12周 |
| 11 | 實驗室檢查,符合要求 |
排除標準包括:
| 1 | 已知肝纖維板層癌、混合型肝細胞癌、膽管細胞癌患者 |
| 2 | 篩選期頭部MRI檢查證實有腦轉移的患者 |
| 3 | 合併門靜脈主乾癌栓堵塞≥50%,或下肢靜脈癌栓 |
| 4 | 首次給葯前5年內診斷為其他惡性腫瘤,除外經過根治的皮膚基底細胞癌、皮膚鱗狀細胞癌和/或經過根治切除的原位癌 |
| 5 | 在本研究治療首次給葯前2周內接受過口服或靜脈給予的有肝癌適應症的中藥製劑或中成藥 |
| 6 | 在首次給葯前4周內接受過肝臟或者其它部位的局部治療(包括經導管肝動脈化療栓塞[TACE]、經導管肝動脈栓塞[TAE]、肝動脈灌注[HAI]、局部放療、放射性栓塞、射頻消融、冷凍消融或經皮乙醇注射等);在首次給葯前4周內進行過肝臟或其他部位的大手術;在首次給葯前1周內接受小手術操作(如單純切除術、拔牙等) |
| 7 | 中度或重度的腹水(需在隨機前1周內經超音波檢查或CT掃描確認),或需要治療性的腹腔穿刺或引流 |
| 8 | 篩選期6個月內發生過經臨床診斷的肝性腦病,採用利福昔明或乳果糖控制的肝性腦病患者不允許入組 |
| 9 | 有出血傾向和血栓史 |
| 10 | 嚴重心血管病史 |
| 11 | 無法控制的活動性感染(CTCAE ≥2級) |
| 12 | HBV檢測顯示HBsAg陽性或HbcAb陽性,且HBV-DNA≥10^4 拷貝數/ml或≥2000 IU/ml(經標準抗病毒治療2周後HBV-DNA不可測的患者可以入組) |
| 13 | 其他實驗室檢查異常 |
| 14 | 妊娠或哺乳期婦女;育齡期女性或男性在研究期間無避孕意願或無避孕措施 |
| 15 | 高敏體質,可能對試驗藥物丙氨酸布立尼布產生嚴重過敏反應的患者 |
| 16 | 在首次服藥前4周內接受過任何在中國未上市的試驗性藥物 |
| 17 | 經研究者判斷認為不適合參與本試驗 |
臨床參加機構(醫院)及主要研究者資訊:
| 序號 | 機構名稱 | 主要研究者 | 國家 | 省(州) | 城市 |
| 1 | 中國人民解放軍第八一醫院 | 秦叔逵 | 中國 | 江蘇省 | 南京市 |
友情提示:
您可以在本公眾號首頁回復關鍵詞「免疫療法」、「肺癌」、「胃癌」、「乳腺癌」、「白血病」、「肝癌」、「腸癌」,獲得相關臨床試驗資訊。
聲明本公眾號文章內容僅供資訊交流使用。如需醫療服務或顧問意見,請向專業人士與機構尋求幫助。
訪問 www.chinadrugtrials.org.cn 輸入本試驗註冊登記號(CTR20180831),可獲得更多詳情。
About us