不想錯過界哥的推送?

晚期卵巢癌該不該行淋巴結清掃術?如何克服卵巢癌的鉑類耐葯?有無新生物標誌準確預測乳腺癌療效?
文丨Cindy
01
晚期卵巢癌行淋巴結清掃術未延長生存,
反而增加死亡風險
系統性盆腔和腹主動脈旁淋巴結清掃術已廣泛用於晚期卵巢癌患者的外科治療,但來自隨機臨床試驗的支持證據有限。那麼,該不該系統地清掃淋巴結呢?

該研究結果發表在最近一期的《新英格蘭醫學雜誌》上。研究提示,接受完全切除術的晚期卵巢癌患者並未從系統性淋巴結清掃術中獲益,相反,淋巴結清掃術導致了治療負擔和對患者的傷害。
研究者表示,該研究結果為長期討論淋巴結清掃術在晚期卵巢癌中的作用提供了1級證據,並再次強調了使用適當的研究方法產生臨床證據的重要性。
據報導,淋巴擴散是早期和晚期卵巢癌的共同特徵及重要預後因素。在包含所有FIGO分期患者在內的未選擇病例系列研究顯示,系統性淋巴結清掃術檢出的淋巴結轉移率為44%~53%。

圖1 總生存和無進展生存
研究納入新診斷的晚期卵巢癌患者(國際婦產科聯合會IIB期至IV期)者,這些患者已接受完全切除術且術前術中淋巴結正常,研究者將其隨機分配行或不行淋巴結清掃術。參與的研究中心有手術技能方面的資格認證。主要終點是OS,次要終點包括PFS、生活質量(EORTC QLQ -C30問卷及卵巢癌模塊QLQ-OV28)以及切除淋巴結的數量。
結果顯示,在2008年12月至2012年1月期間,共有647例患者被隨機分入淋巴結清掃組(323例)或非淋巴結清掃組(324例),並被納入分析。在淋巴結清掃組,切除的淋巴結中位數為57(35個盆腔淋巴結和22個主動脈旁淋巴結)。病理診斷顯示,淋巴結清掃組中有55.7%的患者存在淋巴結微轉移。
-
非淋巴結清掃組的中位OS為69.2個月,淋巴結清掃組為65.5個月(淋巴結清掃組死亡風險比為1.06,95%CI 0.83-1.34,P=0.65)。
兩組的中位PFS也無顯著差異,均為25.5個月(淋巴結清掃組的進展或死亡風險比為1.11,95%CI 0.92-1.34,P=0.29,圖1)。
符合方案人群的敏感性分析證實了這些結果。


圖2 符合方案人群的總生存和無進展生存
兩組患者的生活質量評估未見顯著差異。淋巴結清掃術組的嚴重術後併發症發生率顯著高於非淋巴清掃組,例如,重複剖腹術的發生率(12.4% vs 6.5%,P=0.01)、術後60天內死亡率(3.1% vs 0.9%,P=0.049)。
研究者指出,總體而言,與其他涉及晚期卵巢癌患者手術的3期試驗結果相比,該試驗中的隊列具有相對有利的結果,中位PFS為25個月,中位OS超過5年。在某種程度上,這一發現可能與治療是在專門的外科中心進行等因素有關。
02
AKT激酶抑製聯合化療
可有效治療鉑類耐藥性卵巢癌
臨床前研究顯示,AKT激酶抑製可恢復鉑類耐葯腫瘤的藥物敏感性。臨床研究結果如何?
關於pan-AKT激酶抑製劑Afuresertib聯合紫杉醇和卡鉑(PC)治療複發性鉑類耐藥性上皮性卵巢癌(PROC)和原發性鉑類難治性巢癌(PPROC),英國倫敦帝國理工學院卵巢癌行動研究中心Sarah P. Blagden等進行了的IB期開放標籤、多中心、劑量遞增和擴展研究。
結果顯示,Afuresertib聯合PC方案治療複發PROC有效,Afuresertib的最大耐受劑量(MTD)確定為125mg/d[2]該研究分為兩部分,第I部分是針對複發性卵巢癌的3 + 3劑量遞增研究,以確定Afuresertib的MTD。患者每日連續口服Afuresertib 50-150mg/d,每3周靜脈注射紫杉醇(175mg/m2)和卡鉑(AUC5),共6個周期,然後以Afuresertib 125mg/d維持治療直至疾病進展或發生毒性反應。第II部分是劑量擴展,在複發PROC(A組)或PPROC(B組)患者中單臂評估前述聯合治療的臨床活性。患者口服Afuresertib,(在第I部分中定義的MTD)+PC方案,共6個周期,然後Afuresertib維持治療。主要終點是Afuresertib聯合PC方案的安全性及耐受性(第I部分,劑量遞增),以及根據RECIST 1.1版研究者評估的總緩解率(ORR,第II部分)。
結果顯示,29例患者參加了第I部分研究,30例參加了第II部分研究。觀察到3級皮疹的三個劑量限制性毒性:一個在125 mg,兩個在150 mg Afuresertib。因此,Afuresertib聯合PC方案的MTD被確定為125 mg /d。
研究第I部分中觀察到的最常見(≥50%)藥物相關不良事件包括噁心、腹瀉、嘔吐、脫髮、疲勞和中性粒細胞減少,第II部分中有腹瀉、疲勞、噁心和脫髮。
第II部分治療意向患者的ORR:根據RECIST 1.1標準為32%,根據GCIG CA125標準為52%;中位PFS為7.1個月。
研究者表示,由於新出現的體外數據支持AKT激酶在調節鉑耐葯中的作用,該項研究結果值得進一步研究。在鉑耐葯患者中觀察到的高反應率支持AKT激酶抑製劑可克服化療耐葯的假設。 總體而言,該研究提供了新奇的證據,即AKT激酶抑製聯合化療可有效治療鉑類耐藥性卵巢癌。
03
新乳腺癌生物標誌物
有助選擇最佳治療方案
全世界每年約有210萬女性患乳腺癌,儘管有更好的治療選擇,但超過62.7萬人死於該疾病。基於超過75%乳腺癌是雌激素依賴性的,內分泌治療(也稱為激素治療)是目前最有效的治療方式。但是相當大比例的患者複發且腫瘤似乎對內分泌治療藥物產生耐藥性。
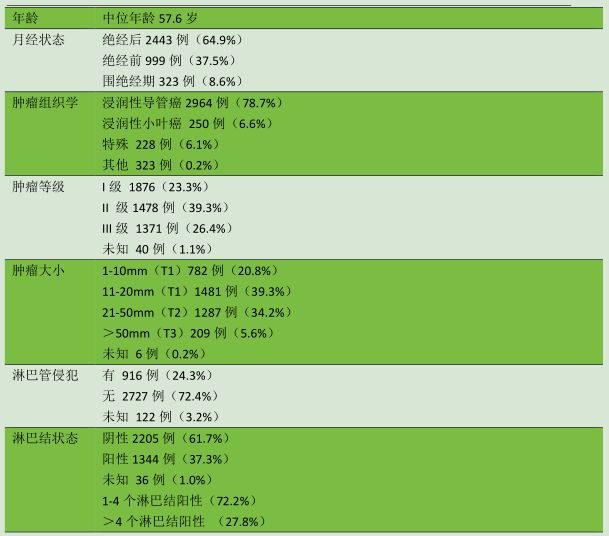
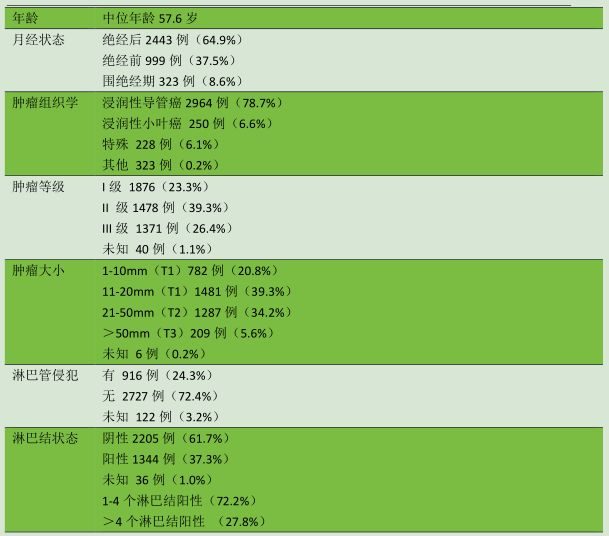
我國東北師範大學遺傳與細胞研究所Dong-Xu Liu和英國諾丁漢大學諾丁漢乳腺癌研究中心Andrew R. Green等[3]開發了一種新的乳腺癌檢測方法,可預測患者對內分泌治療的反應及其複發風險,從而使患者及其醫生能夠做出更好的治療決策。研究顯示,一種名為SHON的癌症相關蛋白與乳腺癌治療反應相關。它準確地預測患者是否會受益於5年抗雌激素治療,以及對化療的反應如何。
先前曾報導,SHON核表達陽性(SHON-Nuc +)可預測雌激素受體α陽性(ERα+)乳腺癌他莫昔芬治療的臨床結果。該研究旨在確定特定單克隆抗體檢測到的SHON表達是否可以提供更準確的預測,並作為基於蒽環類的聯合化療(ACT)的生物標誌物。
結果表明,腫瘤SHON-Nuce +可預測ERα+乳腺癌對他莫昔芬的反應,而SHON細胞質表達陽性(SHON-Cyto +)可預測對ACT的反應。
研究細節
研究者在諾丁漢早期乳腺癌隊列(n = 1,650)中通過免疫組織化學測定SHON表達,如果符合條件,則給予他莫昔芬輔助治療;諾丁漢ERα-早期乳腺癌隊列(n = 697)給予ACT輔助治療;諾丁漢局部晚期乳腺癌隊列給予術前ACT /無紫杉烷(Neo-ACT,n = 120),若符合條件,給予5年他莫昔芬輔助治療。分析SHON的預後意義及與治療臨床結果的關係。
結果顯示,如先前報導,排除他莫昔芬輔助治療後,在高危/ERα+患者中,與SHON-Nuc-相比,SHON-Nuc +與死亡風險降低48%顯著相關(HR=0.52,p= 0.002)。同時,在接受輔助ACT相比治療的ERα-患者中,與SHON-Cyto-相比,SHON-Cyto +與死亡風險降低50%顯著相關(HR=0.50,p=0.0003)。
在接受Neo-ACT治療的患者中,SHON-Nuc-或SHON-Cyto +分別與SHON-Nuc +(21% vs 4%,p=0.012)或SHON-Cyto-(20.5% vs 4.5%,p=0.017)相比,病理完全緩解(pCR)率顯著增加。
接收Neo-ACT治療後,與SHON-Nuc-患者相比,SHON-Nuc +患者遠處複發風險明顯更低(HR=0.41,p=0.038),而SHON-Cyto +患者相比SHON-Cyto-患者有明顯更高的遠處複發風險(HR=4.63, p=0.043)。
此外,多變數Cox回歸分析顯示,SHON-Cyto +與Neo-ACT和5年他莫昔芬治療後的遠處複發風險更高獨立相關(HR=5.08,p=0.037)。ERα狀態與SHON-Nuc +(p=0.005)之間以及SHON-Nuc +與他莫昔芬治療之間(p=0.007)的相互作用均具有統計學意義。
研究意義
研究者表示,該研究清楚地證明,腫瘤SHON表達是他莫昔芬和化療反應的潛在生物標誌物。這將為醫生及其患者提供可靠的預測工具,以便做出最有效的治療選擇。
但對SHON確切機制仍不清楚。在明確其作用機制中,識別潛在的SHON受體並確定SHON在雌激素受體陰性乳腺癌中的作用將是下一個優先事項。在臨床實施該測試之前,需要進行更多的研究。
參考文獻
[1] Harter P, Sehouli J, Lorusso DA, et al. Randomized Trial of Lymphadenectomy in Patients with Advanced Ovarian Neoplasms[J]. N Engl J Med. 2019;380(9):822-832.
[2] [2]Blagden SP, Hamilton AL, Mileshkin L, et al. Phase IB Dose Escalation and Expansion Study of AKT Inhibitor Afuresertib with Carboplatin and Paclitaxel in Recurrent Platinum-resistant Ovarian Cancer[J]. Clin Cancer Res. 2019;25(5):1472-1478.
[3]Abdel-Fatah TMA, Broom RJ, Lu J, et al. SHON expression predicts response and relapse risk of breast cancer patients after anthracycline-based combination chemotherapy or tamoxifen treatment[J]. Br J Cancer. 2019 Feb 28. [Epub ahead of print]
覺得好看,請點這裡
↓↓↓↓