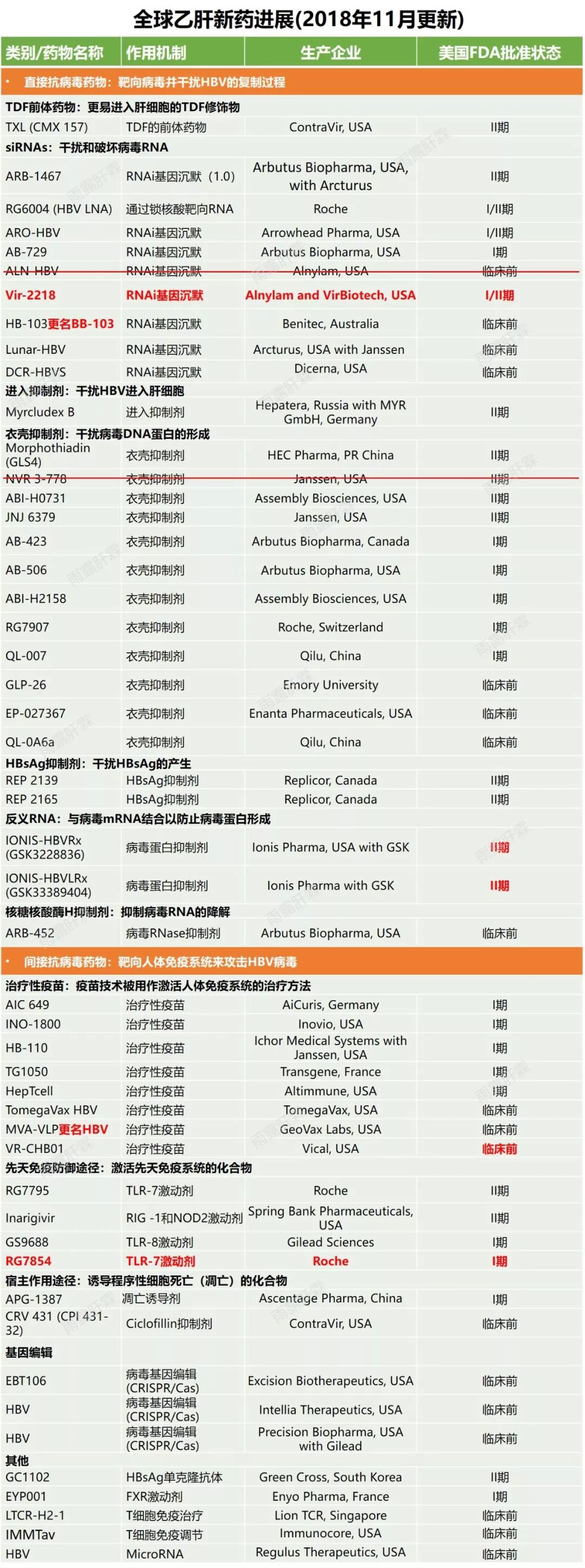
還記得昨日小番健康曾經介紹,生物技術公司(Vir Biotechnology)正有2種在研B肝新藥分別為VIR-2218和VIR-3434處於臨床開發階段,並且預計下半年將啟動三項2期聯合用藥臨床試驗,VIR公司宣布,正式啟動2期VIR-2218+VIR-3434組合!(可見下圖:來自VIR,啟動2期評估VIR-2218和VIR-3434組合作為慢B肝病毒感染功能性治愈方案)

B肝在研新藥VIR-2218+VIR-3434,2期組合,首位受試者完成給藥
根據VIR公司介紹,這項2期臨床試驗指MARCH(抗B肝單克隆抗體siRNA組合)已經在第一位受試者中完成給藥。這是一項多中心、開發標簽的2期臨床試驗,旨在評估VIR-2218和VIR-3434組合,在大約90名曾經接受核苷類逆轉錄酶抑製劑治療的成年慢性HBV感染患者(18至65歲)中進行。
2期VIR-2218和VIR-3434組合設計,將在試驗過程中,以不同劑量水準通過皮下注射給藥,治療期是4至20周,隨訪期長達116周,具體將取決於給藥隊列。這項在研B肝新藥聯合2期臨床試驗的主要終點是,出現治療突發不良事件和嚴重不良事件的患者比例;治療後的臨床實驗室參數分級;以及實現功能性治愈(定義為B肝表面抗原檢測不到和HBVDNA持續抑製)的患者比例。

來自VIR公司的首席醫療官,醫學博士Ph.Pang原文點評如下:B肝病毒感染仍然是一個緊迫的全球公共衛生挑戰,我們相信專注於免疫恢復的聯合方法對於實現功能性治愈是至關重要的。我們對VIR-2218作為這項組合方案的基石潛力感到興奮。將VIR-2218和VIR-3434進行聯合使用,而VIR-3434正在進行第1期臨床試驗,已經證明其能夠顯著地將B肝表面抗原降至較低水準,最重要的是,它具有作為治療性T細胞疫苗的潛力,這有可能改變目前HBV藥物現狀。
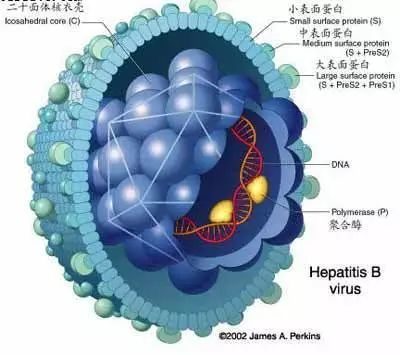
VIR-2218是一種還未上市,正處於臨床研究的小干擾核糖核酸(siRNA),旨在抑製所有HBV蛋白(X、聚合酶、S和核心蛋白)的產生,這些蛋白可能充當免疫耐受原。VIR-3434也是一種還未上市,正處於臨床研究階段的HBV中和單克隆抗體,旨在阻止所有10種B肝病毒基因型進入肝細胞,並降低血液中病毒粒子和亞病毒顆粒的水準。它還經過Fc工程技術改良,包括XX2“疫苗突變”,使其有可能用作針對HBV的治療性T細胞疫苗。

從研發特點來看,VIR-2218是一種在研的皮下注射靶向B肝病毒小干擾RNA分子,有著刺激有效免疫反應的潛力,且具有針對B肝病毒的直接抗病毒活性。它也是VIR公司B肝新藥臨床項目中,第一個包含增強穩定化學加(ESC+)技術的siRNA,這種技術可以增強穩定性並最大限度地減少脫靶活性,可能導致治療指數增加。VIR-2218還是VIR公司與Alnylam Pharmaceuticals合作並進入臨床研究的資產。
VIR-3434是一種在研的採用皮下注射的HBV中和單克隆抗體,被Fc工程技術設計成可能用作抗B肝的T細胞疫苗,即一種正處於臨床研究階段的治療性B肝疫苗。它還結合了Xencor的 Xtend™以延長半衰期。

小番健康結語:VIR公司宣布,已經啟動2期臨床試驗,以評估作為慢性B肝病毒感染的VIR-2218(RNAi技術)+VIR-3434(治療性B肝疫苗)的組合方案,目前,該2期已經完成對第一位患者的給藥!返回搜狐,查看更多
責任編輯: