導語:被譽為人類的"第二基因組"的腸道菌群,近年來已經成為最火爆的研究領域之一。有研究表明,腸道細菌可以加速阿爾茨海默病的發展。
近日,腸道細菌重出江湖,再顯神威,研究人員首次發現,小鼠腸道革蘭氏陰性菌感染可誘發帕金森病的發生發展。在缺失帕金森病相關基因Pink1的小鼠中,輕微的腸道感染就能引髮針對多巴胺神經元的異常免疫反應,並導致小鼠成年後出現帕金森樣運動障礙。


帕金森氏病(Parkinson氏病)是伴有運動障礙的神經退行性疾病,已被證實其與黑質內核團多巴胺能神經元缺失有關,但其具體發病機制仍是未解之謎,而大量研究表明大約10%的PD病例是由於編碼PINK1和Parkin等蛋白質的基因突變所致。
Parkin最早在青少年Parkinson氏病的研究中被發現,現有模型認為,PINK1可磷酸化激活Parkin和泛素分子,使應激後損傷的線粒體發生泛素化修飾,經線粒體自噬途徑(Mitophagy)完成降解清除。
儘管目前已證實PINK1和Parkin突變可引起Parkinson氏病,但Pink1?/?和Prkn?/?的小鼠模型卻幾乎未見有Parkinson氏病樣運動障礙發生,研究人員猜測,小鼠模型的無菌環境是該現象的主要原因,於是他們給小鼠餵了大量的細菌,神奇的一幕發生:小鼠們發病了。
以往的流行病學和基礎研究表明,自身免疫反應極有可能是帕金森病的背後推手,而以上發現給研究人員提供了靈感:或許腸道細菌的感染恰好是帕金森的免疫扳機觸發點,通過誘導線粒體抗原呈遞過程(mitochondrial antigen presentation,MitAP)引起CD8+T細胞發生線粒體特應的活化。


PINK1/Parkin的缺失導致MitAP
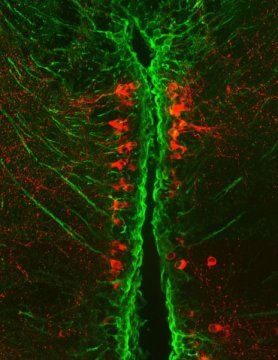
為證實這一推測,研究人員在Raw 264.7細胞內表達了糖蛋白gB(glycoprotein B)以指示抗原呈遞,並植入多種細菌,果然,只有革蘭陰性菌可引起MitAP。隨後,研究者分離了感染小鼠的脾細胞,發現Pink1敲除小鼠的抗原提呈細胞裡出現了MitAP,產生了針對線粒體的殺傷性T細胞。
既往已有研究發現LPS可誘導多巴胺能神經元表達MHC-I分子,使其易感於CD8+T細胞的免疫作用。研究人員在體外共培養中發現,與Pink1?/?小鼠神經元共培養可誘導雜交瘤細胞發生MitAP,並在共培養5天后發現40%多巴胺能神經元死亡。這些結果提示,在Pink1?/?小鼠感染模型中,發生了MitAP的CD8+T細胞在腦中浸潤增加,進而引起多巴胺能神經元死亡。
機制搞清楚了,所以小鼠們到底有怎樣的表現呢?
在吃了革蘭陰性菌之後,小鼠感染不嚴重,20天左右就完全康復;但是在感染4個月以後,Pink1敲除小鼠開始「不會走路」了。很明顯它們全身都不太靈活,特別是後腿,頭也抬不起來,而給予左旋多巴後,小鼠又生龍活虎了!
本研究的關鍵之處在於將腸道感染模型引入到Parkinson氏病動物模型的研究中,從而解釋了既往Pink1?/?小鼠因缺少炎症性乾預而未有Parkinson氏病癥狀的原因。
神經退行性疾病的發生並非是單一因素促成,而是遺傳、神經病理、感染免疫乃至更多因素共同參與的病理過程。該發現為帕金森的研究開闢了新思路,也為帕金森的治療帶來了全新的方向和可能性。
參考文獻