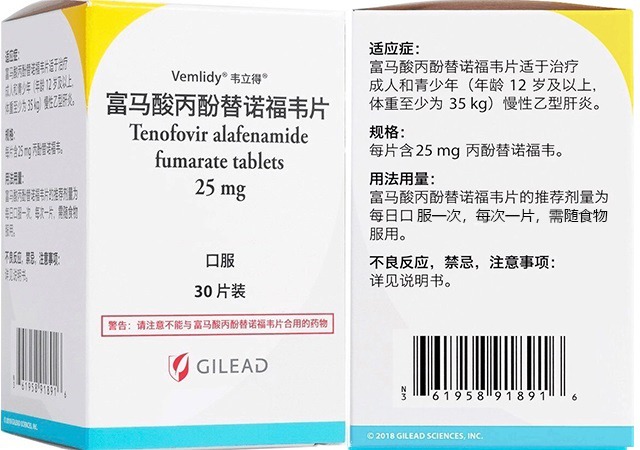
2020年8月11日首次發布並更新的一項臨床試驗,試驗題目(英譯):TAF治療孕婦慢性乙型肝炎的療效及安全性分析。本試驗是使用富馬酸替諾福韋艾拉酚胺(TAF)25毫克的早期階段研究,目的是探討TAF作為一種新上市抗病毒藥物,在預防孕期母嬰傳播的有效性和產後安全性。

B肝替諾福韋艾拉酚胺試驗,考察特定人群, 12月30日完成
試驗背景基於當前對孕期母嬰傳播的預防和產後有效性方面,富馬酸替諾福韋艾拉酚胺(TAF)治療還沒有一些明確相關數據支撐。新版《慢性B肝防治指南》也認識到母嬰阻斷對於妊娠中晚期孕婦的有效性(來自本試驗研究人員點評)。TAF是一種新上市B肝抗病毒藥物,為了了解其對女性孕期預防母嬰傳播和產後有效性,因此,研究人員啟動本研究。
本研究臨床試驗編號:NCT04507607,登記於全球臨床試驗庫,研究開始時間:2020年8月1日,預計初步完成時間:2020年12月30日,預計本研究整體完成時間:2021年6月30日,由我國中山大學第三附屬醫院主辦。符合條件者需經過中山大學第三附屬醫院感染門診診斷後,方可入本院小組,每位入組前需簽署知情同意書。

本試驗設計招募50名,手臂乾預/治療,實驗性:患有慢性B肝的孕婦,從懷孕24周開始服用TAF直到分娩。每月複查肝功能、病毒載量以及抗原情況,收集外周血10ml。藥物:富馬酸替諾福韋艾拉酚胺25毫克,在妊娠期間,對患有慢性B肝的孕婦進行TAF治療。女性未懷孕的慢性B肝患者接受TAF抗病毒治療。
主動對照:慢性B肝婦女,接受TAF抗病毒的非妊娠婦女定期複查肝功能、病毒載量以及抗原。藥物:富馬酸替諾福韋艾拉酚胺25毫克,在妊娠期間對患有慢性B肝的孕婦進行TAF治療。女性未懷孕的慢性B肝患者接受TAF抗病毒治療。試驗設計主要結果指標:產時肝髒指標、出生時孕婦的肝功能(ALT、AST)、HBV-DNA、HBV血清學標誌物(HBsAg、HBeAg、HBeAb)水準變化;

產後12個月的肝髒指標、孕婦分娩後1個月、3個月、7個月、9個月、12個月肝功能(ALT、AST)、hbvdna、HBV血清學標誌物(HBsAg、HBeAg、HBeAb)水準的變化。次要結果指標:妊娠24周至分娩的妊娠肝指標;應用TAF的0、4、8、12周孕婦肝功能(ALT、AST)、HBV-DNA、HBV血清學標誌物(HBsAg、HBeAg、HBeAb)水準的變化。
入選標準:18到60歲成人女性,符合符合《慢性乙型肝炎防治指南》診斷標準的HBeAg(+),HBV-DNA大於或等於2×10^6IU/mL的孕婦為妊娠24~28周的孕婦。符合《慢性乙型肝炎防治指南》診斷標準的25例HBeAg(+),HBV-DNA大於或等於2×10^6IU/mL的非孕婦。入組患者均為未經治療的新入院患者,完成相關檢查後不符合標準的,將予以剔除。

排除標準:與HAV、HCV、高密度肝炎病毒、HEV或HIV混合感染;有抗病毒治療或與免疫調節藥物、抗腫瘤藥物、細胞毒性藥物或免疫抑製性類固醇同時治療的病史;三維超聲顯示胎兒畸形;配偶感染B肝病毒;失代償性肝病病史(如伴有凝血障礙的失代償性肝病、高膽紅素血症、肝性腦病、低蛋白血症、腹水和食管靜脈曲張出血)、肝癌或其他慢性肝病(如自身免疫性肝炎)或臨床症狀的病史;免疫疾病史;有嚴重心血管疾病史;研究人員認為不適合參與試驗的其他原因。以上信息登記於全球臨床試驗數據庫,試驗題目:TAF治療慢性乙型肝炎感染孕婦的療效和安全性。返回搜狐,查看更多
責任編輯: