近年來,免疫治療在腫瘤治療領域「大爆發」。其中,基因治療在腫瘤免疫治療方面得到越來越廣泛的應用。溶瘤病毒,作為基因治療中攻克實體瘤的一種獨特的手段,有望成為消滅癌症的希望。
溶瘤病毒抗腫瘤發現歷程
早在一個多世紀前,人類發現自然界存在的一部分天然病毒株感染人體後能溶解破壞腫瘤細胞,引起腫瘤的消退。膽大的醫生開始嘗試用病毒治療腫瘤,但一直沒有實質性的進展,野生病毒株的病原性和致病性很難得到有效控制。
溶瘤病毒來源於兩大類病毒。
一種是天然病毒株,天然具有在癌細胞中複製的特性,例如自主細小病毒、粘液瘤病毒等,其實這類未經改造的天然病毒,針對腫瘤的特異性是有限的。
另一種是基因改造的病毒株,經基因改造優化而具有腫瘤選擇性殺傷的特異性,包括麻疹病毒、脊髓灰質炎病毒、痘苗病毒、腺病毒、單純胞疹病毒、牛痘病毒等等。這類病毒基因組結構差別很大,改造的空間也大,是溶瘤病毒研發的重要方向,也是最有潛力的一類。
基因工程改造溶瘤病毒
隨著現代醫學和生命科學的發展以及基因工程技術的提高,可以對病毒基因組進行改造,這才使溶瘤病毒重新回到科學家的視野,溶瘤病毒治療癌症也有了可能。


溶瘤病毒通過基因工程方法,改造活的、天然存在的、感染人體細胞的野生病毒,用於治療各種實體瘤,例如肺癌、肝癌、皮膚癌、乳腺癌等,憑藉殺傷率高、靶向性好、副作用小、能在感染的腫瘤細胞中複製繁殖並殺死腫瘤細胞等優勢,發展成為當今腫瘤免疫療法的重要手段之一。
溶瘤病毒的殺瘤機制
溶瘤病毒發揮對腫瘤細胞的殺傷作用主要通過以下途徑:
(1)直接裂解腫瘤細胞;
(2)病毒感染的腫瘤細胞表達相關信號並釋放大量細胞因子造成免疫細胞對腫瘤細胞浸潤;
(3)裂解的腫瘤細胞釋放特異性抗原和免疫相關因子,誘發機體產生抗腫瘤免疫反應;
(4)溶瘤病毒可以作為載體攜帶腫瘤抑製基因、促凋亡基因、抗血管生成基因、自殺基因和免疫調節基因,調控腫瘤免疫耐受微環境。


經過基因工程技術處理過的病毒已經失去了病源性,但是仍保留這感染性,可以只針對腫瘤細胞進行感染,裂解癌細胞,因此在人體內是安全的,有強大的殺瘤效果。既可以應用於全身也可以用於局灶治療。
溶瘤病毒對抗腫瘤有哪些優勢?
溶瘤病毒本身具有破壞腫瘤細胞作用,它也可以作為載體攜帶抗癌基因,隨著溶瘤病毒在腫瘤細胞內的複製,抗癌基因的拷貝數也跟著複製而成千萬倍增加,其表達量也必然得到加強,再加上病毒體積小、彌散力強的優點,可以在腫瘤原發灶及轉移灶局部形成高濃度病毒,達到殺滅腫瘤細胞的目的。


只要有腫瘤細胞存在,就能啟動溶瘤病毒的複製,繼續產生腫瘤殺傷效應。在基因調控元件的嚴謹調控下,改造後的溶瘤病毒在正常細胞內不具有複製的能力,因而對正常細胞不會產生影響。
經過多年的臨床應用,沒有發現溶瘤病毒嚴重的毒副作用,證明了溶瘤病毒的臨床應用還是比較安全的。
另外,研究發現溶瘤病毒不僅能增強放化療作用,其感染腫瘤細胞後釋放大量細胞因子,裂解的腫瘤細胞釋放大量腫瘤相關抗原,都有抗腫瘤免疫激活作用,因此,溶瘤病毒也是腫瘤免疫治療的重要組成部分。
首次獲批溶瘤病毒療法的國家是中國!
安柯瑞,於2005年4月被中國國家藥品監督管理局批準上市,它是一種進行基因重組而得的溶瘤腺病毒,主要用於治療晚期鼻咽癌。
安柯瑞是全球首個上市的、溶瘤病毒免疫治療類抗腫瘤藥物,開創了人類利用病毒治療腫瘤的先河,也使得中國成為世界上第一個成功利用基因工程手段開發抗腫瘤藥物新領域——腫瘤溶瘤免疫療法的國家。


T-vec(Imlygic),於2015年10月被美國FDA批準上市,它是一種對單純皰疹病毒進行改造而得的病毒,主要用於治療晚期黑色素瘤。目前T-Vec已在美國、歐洲和澳大利亞廣泛用於複發黑色素瘤治療。
其實,另外兩種也應該算是溶瘤病毒藥物。2003年,重組腺病毒-p53抗癌注射液(今又生)獲得中國原CFDA批準,成為世界上首個獲準上市的基因治療癌症藥物;2004年,非致病性的人腸道細胞病變孤兒病毒(enteric cytopathic human orphan virus)--RIGVIR,在拉脫維亞獲批用於治療黑色素瘤。
至今,溶瘤病毒獲得了哪些治療進展?
黑色素瘤篇
①溶瘤病毒聯合PD-1有效率達62%!
溶瘤病毒可以將現有的免疫治療結合,協助T細胞在局部腫瘤微環境中的增殖,加強免疫治療的療效。
2017年,《Cell》報導,研究人員表示,耐受PD-1的病人腫瘤內部往往缺少CD8+的T細胞。因此,通過其他免疫療法促進CD8+的T細胞對腫瘤的浸潤也許能提高PD-1抗體的療效。於是設計了一個聯合用藥方案,先直接注射溶瘤病毒T-VEC到黑色素瘤病灶,再靜脈輸入PD-1抗腫瘤藥物(派姆單抗)。


結果非常驚艷,T-Vec聯合PD-1抗體派姆單抗治療腫瘤有效率為62%,其中33%為完全緩解,而單用T-Vec、PD-1抗體僅為40%和35%。
②術前聯合溶瘤病毒治療,複發率大大降低!
2019美國ASCO年會上,PMC希爾曼癌症中心主任Robert L. Ferris博士公布一項隨機試驗結果,對於可切除的晚期黑色素瘤患者,與單獨手術相比,新輔助(即手術前添加)溶瘤病毒療法(T-Vec;Imlygic)可以使得1年無複發生存率的顯著改善。


150名患有高風險、可切除的IIIB-IVM1A期黑色素瘤的患者隨機分成兩組,即刻手術或病灶內注射T-Vec,然後在第13周進行手術。結果顯示聯合溶瘤病毒組無複發生存率33.5%,單獨手術組僅21.9%。術前新輔助溶瘤病毒療法T-Vec病理完全緩解率為21%,客觀緩解率為14.7%。
三陰乳腺癌篇
溶瘤病毒療法曙光初現,未來可期!
在2019年AACR年會上發表的一項小型的研究表明,大多數三陰乳腺癌的患者在接受基因型溶瘤病毒(T-VEC,Imlygic)和新輔助化療治療後均獲得病理完全緩解(pCR)。


1期研究中,將溶瘤病毒(T-VEC)聯合化療應用於乳腺癌患者身上,9名患者中有5名達到完全緩解,其餘4名患者只有很小的殘留病灶。
Moffitt癌症中心醫學博士Hatem Soliman博士說:「即使在某些腫瘤可能無法通過新輔助化療完全消退的情況下,當溶瘤病毒與治療結合使用時依然能夠解決。」
基於1期試驗的優異數據,該研究中心將會開展2期臨床試驗,進一步探索溶瘤病毒在三陰乳腺癌治療的作用。
結直腸癌篇
三聯療法根除所有小鼠結腸癌細胞!
2018年12月,一項早期研究表明,溶瘤病毒T-VEC與分子靶向藥物MEK抑製劑(曲美替尼)聯合使用可顯著增強黑色素瘤治療反應和腫瘤細胞殺傷,並且在該方案中加入PD-1抑製劑可進一步改善治療反應,在小鼠模型中達到近100%的腫瘤消退。
這項研究於2018年12月12日發表在Science Translation Medicine,通訊作者為麻省總醫院(MGH)外科腫瘤科和溶瘤病毒公司Replimune的首席醫療官Howard L. Kaufman博士。他在一份聲明中說:「我們使用的所有三種藥劑都已獲得FDA批準,研究為它們的聯合使用提供了理由,應該優先考慮一項檢驗這種三藥方案的臨床試驗」。


研究人員還在結腸癌小鼠模型中測試了雙重和三重組合,並觀察到相似的結果:當T-VEC與Trametinib或抗PD-1聯合使用時,存活率顯著提高,但三聯組合根除了所有治療結腸癌小鼠的腫瘤。
實體瘤篇
TILT-123聯合PD-L1進軍實體瘤,前期有效率100%
TILT Biotherapeutics是一家致力於利用溶瘤病毒增強包括免疫檢查點抑製劑在內腫瘤T細胞療法的生物技術公司。近日,該公司宣布與默克和輝瑞達成合作協議,評估其溶瘤病毒TILT-123聯合PD-L1腫瘤免疫療法Bavencio(avelumab)治療對常規療法難治的實體瘤患者。



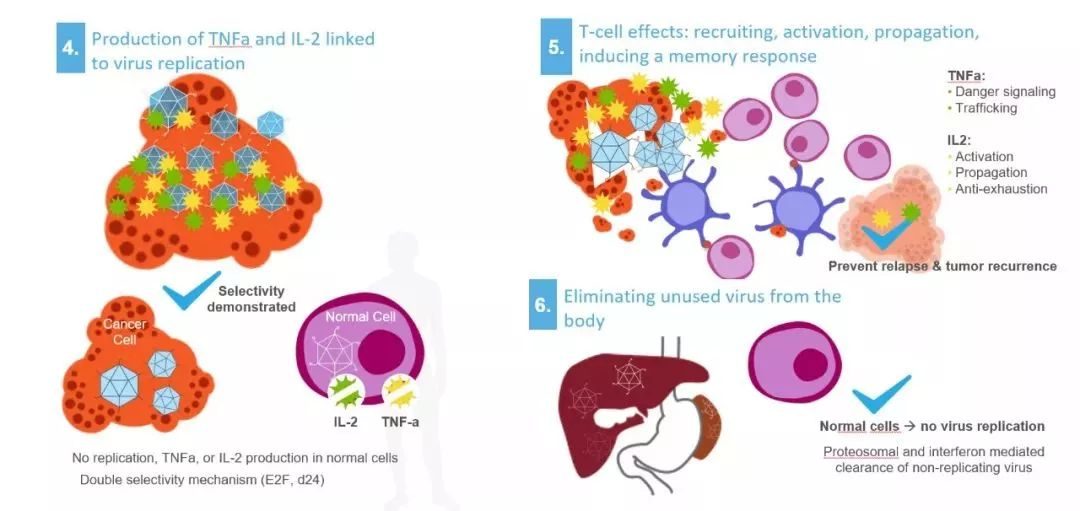
TILT-123的作用機制(圖片來源:TILT公司官網)
TILT-123僅選擇性地在癌細胞中複製並在腫瘤局部產生免疫刺激性細胞因子(TNFA和IL-2)的,這在不同的體內和體外研究中得到證實。該產品已被精心設計可增加對癌細胞的侵入,其給葯可以通過系統和局部途徑,使其有可能適用於各種癌症的治療。
來自TILT技術的臨床前數據(單用或聯用其他免疫治療藥物,如T細胞和檢查點抑製劑)已顯示出100%的有效率。
寫給癌症患者
目前,溶瘤病毒以瘤內注射為主,多於用體表腫瘤或部位局限腫瘤,限制了其臨床應用範疇。若可以實現系統性給葯(如靜脈注射)會有更大的臨床價值,有望治療轉移性腫瘤或血液腫瘤。
專家表示溶瘤病毒對腫瘤細胞殺傷效率高、靶向性好、安全性高、副作用小、成本低廉,應該能成為未來最具有潛力和應用前景的惡性腫瘤治療手段之一。溶瘤病毒治療及臨床試驗入組諮詢電話400-626-9916
國內、國外多家癌症治療機構及團隊一直在癌症溶瘤病毒治療領域精耕細作,持之以恆,探索溶瘤病毒聯合其他靶向治療或者免疫治療,獲得更大的臨床應用價值。