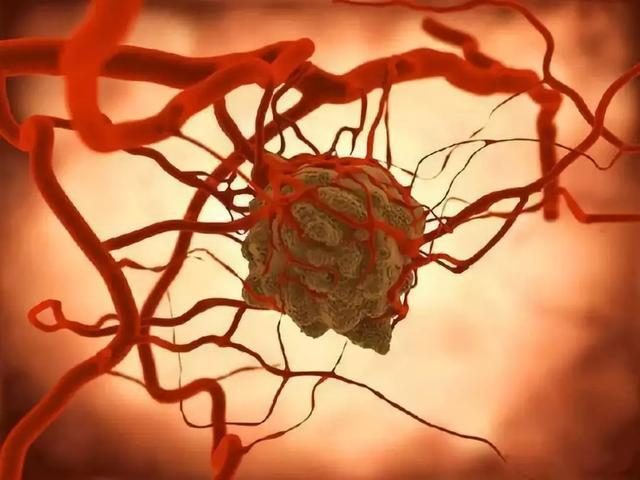
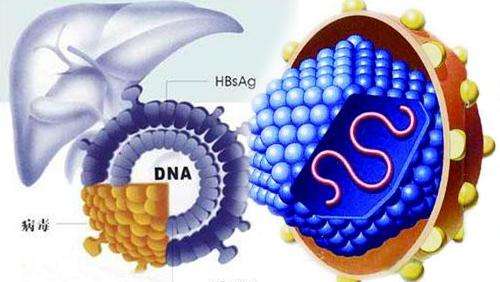
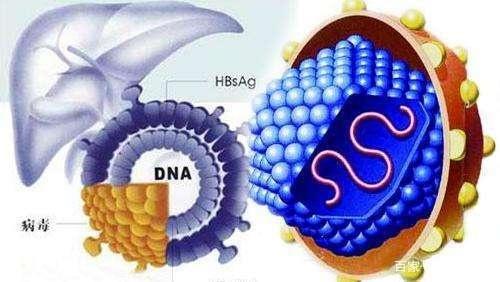
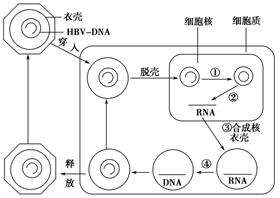
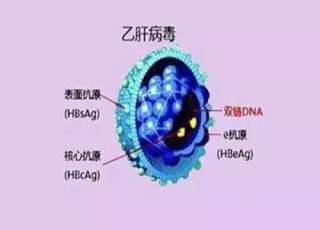
B肝表面抗原,也稱為澳大利亞抗原,最早被發現至今已近60年,病毒性肝炎依然是肝硬化和肝細胞癌發病和死亡主要原因。現有一線批準藥物包括干擾素α,聚乙二醇干擾素α、恩替卡韋(ETV)、富馬酸替諾福韋酯(TDF)以及富馬酸替諾福韋艾拉酚胺(TAF)。

B肝候選藥物設計,大多數是小分子,阻止HBV複製不同階段
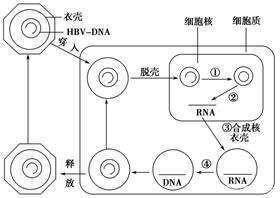
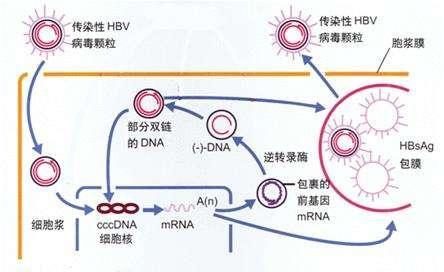
其中,ETV/TDF/TAF均屬於NAs,雖然NAs抑製病毒複製的轉錄後階段,但它們並不以穩定持續存在的共價閉合環狀DNA(cccDNA)作為靶點。因此,比如NAs這一類已授權上市抗病毒藥物,在病毒學方向有局限性。cccDNA,這是B肝病毒複製的中間體,它是在肝細胞的細胞核內形成的一個小染色體,並可能發生表觀遺傳修飾。
而B肝病毒的X蛋白(HBx),它通過滅活染色體結構來維護複合體的組成部分,發揮cccDNA的穩定作用。cccDNA和宿主轉錄因子和病毒蛋白結合,使病毒基因表達和複製。與調節甲基化或異染色質形成的因素相關,也可能讓cccDNA失活,並導致持續潛伏或隱匿的HBV感染。越來越多研究表明,B肝病毒的逃逸突變進展或免疫缺陷,都可能導致HBV複製重新激活,因此,全球科研人員強調cccDNA特異性治療藥物開發是有必要的。

目前,B肝領域大多數候選藥物都是小分子藥物,主要目的是在阻止HBV複製的不同階段。新一代NAs的設計思路方向,主要是可以抑製病毒聚合酶,降低毒性,提高HBV的耐藥屏障。其他正在開發的直接作用抗病毒藥物包括HBV核心蛋白變構調節劑、HBV表面抗原(HBsAg)釋放抑製劑和核酸聚合物,也可以抑製B肝病毒進入。
隨著全球科研人員發現了牛磺膽酸鈉共轉運多肽(NTCP)有助於HBV進入肝細胞,肽抑製劑比如Myrcludex-B也被開發用於單純HBV或HBV/HDV共感臨床試驗。基因新療法方向,上一期小番健康已經介紹了RNAi分子,雖然HBV治療領域研發藥物前景廣闊,但目前還很少有直接能夠禁用cccDNA的方法被開發出來。目前,最接近的方法是,序列特異性RNA引導核酸酶(RGN)和蛋白質的靶向誘變,這種方法已經引起人們興趣。

因為這種方法可以通過永久地禁用cccDNA,從而治愈HBV感染(基因為基礎靶向cccDNA新療法)。HBV cccDNA是核酸酶基因編輯的主要候選基因,因其微染色體結構和有限序列具有可塑性。雖然病毒逆轉錄酶保真度較低,但緊湊的病毒基因組和重疊的閱讀框,限制了逃逸突變體發展。病毒基因組內的插入和缺失,可能導致異常或截斷蛋白,進而干擾病毒複製。
鋅指蛋白(ZFs)是豐富的多功能哺乳動物蛋白,它作為轉錄因子自然發生。通過特異性靶向單個ZFs的核苷酸三聯體,這些蛋白可以被設計成具有特定DNA結合特性的陣列。過往研究表明,抗HBV ZFNs首次在一個概念驗證實驗中被描述,其中36%的質粒來源的病毒序列,在病毒複製的細胞培養模型中被破壞。

與ZFNs一樣,talen是一種核酸酶二聚體,由DNA結合蛋白與核酸內切酶結構域融合而成。轉錄激活因子樣效應(TALE)來自於黃單胞菌,其個體重複結構域包含33-35個氨基酸,可識別單個鹼基對。這些重複序列的核苷酸結合特異性由位於12和13位的重複可變雙殘基(RVDs)決定。在以往曾有科學動物實驗表明,核酸酶的體內抗病毒作用,沒有發現肝髒毒性,以及觀察到血清B肝表面抗原和環狀病毒顆粒顯著下降。返回搜狐,查看更多
責任編輯: