全球還有一些具有吸引力的潛在B肝藥物靶點,如核受體(NRs),針對NR的方法來開發HBV藥物也是未來有機會進入臨床前研究的。小番健康簡單介紹一下,核受體是什麽,這些核受體之間相互作用對於B肝科研工作有哪些意義,以及針對B肝病毒轉錄的一些藥物發現前景。

B肝藥物發現,NRs或HNF4α,有望作為潛在有吸引力靶點
目前已知的核受體共有48個,是後生動物(指除原生動物之外所有其他動物)中最豐富的轉錄介質超家族。這些核受體主要是由配體-受體之間相互作用觸發,並可以作為參與細胞增殖、代謝與體內平衡的轉錄因子來發揮作用。
核受體和一個或多個可變反式激活域共享一個規範的結構組織。這些包含保守的DNA結合域、包括靈活鉸鏈核定位信號與C端配體結合域。當它們被內源性或外源性配體刺激之後,受體二聚化為同源二聚體或異源二聚體。一般而言,它們還和來自不同亞家族的兩種成分形成異二聚體。根據現有就受體和配體之間已知結合譜,科學家可以通過計算機輔助藥物設計,簡單的生成模仿配體的小分子。
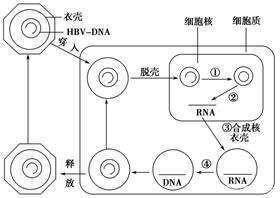
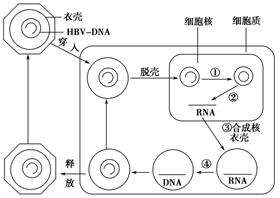
以上介紹的這種獨特的NRs小分子,正是在今後B肝潛在的藥物靶點,它是針對核受體來開發藥物的。目前,關於B肝病毒基因組整合體的基因轉錄了解程度,全球科研人員對此掌握得都比較有限。B肝病毒整合子隨機分布在整個宿主基因組之中,還沒有任何證據可以表明,優先整合位點或與特定基因類別相鄰。簡言之,整合體的轉錄是獨立發生的,和cccDNA介導的病毒複製沒有關係。

在針對B肝病毒轉錄這個方向,IFN-α是一種已獲批的抗病毒治療劑。這種方法的作用機理並不是直接抑製HBV複製,而是干擾素刺激基因(ISG)誘導的,其蛋白質產物具有廣泛的抗病毒活性。都知道B肝病毒生命周期中存在多個步驟,而ISG可以發揮一系列不同的機理,來控制HBV複製。IFN-α策略誘導STAT1/2募集到抑製轉錄的cccDNA上。細胞因子通過在體外和人源化小鼠中調節其表觀遺傳修飾,來起到抑製cccDNA的轉錄效果。
促炎性白細胞介素 6 (IL-6) 在受感染的HepG2NTCP細胞中,抑製來自cccDNA的pgRNA與preS/S轉錄。重組IL-6 (rIL-6) 處理將HNF1α和HNF4α與cccDNA 分離,它們兩者都屬於上面介紹的轉錄所必需元素。 rIL-6誘導STAT3的整體磷酸化;與IL-6 細胞靶基因相比,cccDNA上募集的磷酸化STAT3水準較低。這種重新分布是可以導致B肝病毒轉錄減少。

轉化生長因子 (TGF-β) 處理誘導活化誘導的胞苷脫氨酶 (AID) 的表達,並在較小程度上誘導APOBEC3F和3G,但不會誘導APOBEC3A。AID與HBVRNA關聯,可以並入核衣殼中,B肝病毒pgRNA在其中脫氨基。AID介導的病毒減少是以聚合酶依賴性方式發生,這需要AID和聚合酶之間存在物理關聯。這種相互作用進一步介導了RNA外泌體蛋白的募集。
在上面提及的IFN-α、IL-6相近,轉化生長因子 (TGF-β) 也能夠顯著下調HNF4α表達和核心啟動子活性,進而導致pgRNA量的減少。以上這些重要發現,都被科學家將HNF(尤其是HNF4α)視為今後HBV領域具有吸引力的藥物靶點!這類藥物靶點設計方向是,通過阻斷HNF活性或將其與cccDNA分離的藥物製劑,可能有助於抑製來自cccDNA的病毒基因轉錄。

小番健康結語:讀者朋友應加以區分藥物發現:核受體(NRs)和細胞因子應對HBV轉錄方法,HBV轉錄細胞因子主要有三種方向,即已獲批IFN-α、促炎性白細胞介素 6 (IL-6) 和轉化生長因子 (TGF-β) ,HNF4α可能成為未來有希望的HBV藥物靶點來設計,因為目前科學家發現,阻斷HNF活性可能抑製來自cccDNA的病毒基因轉錄!返回搜狐,查看更多
責任編輯: