B肝抗病毒藥物方向,相關領域科研人員若選擇以核苷(酸)類似物繼續開發,該方向未來發展應集中在降低毒性、增加水溶性以及降低耐藥風險。除了發掘廣譜抗病毒藥物外,干擾素研發設計方向更重要還是應該體現在,以最小毒性的發展高選擇性干擾素。
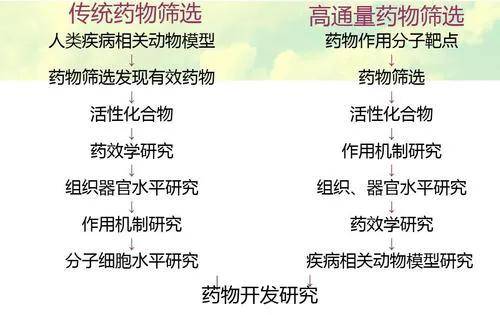
B肝以往藥物,圍繞HBVDNA聚合酶,其他分子正積極開發中
目前,全球已獲批用於HIV感染的化合物有25種,但目前真正獲批用於HBV感染治療藥物只有8種。HBV領域,它們分別是干擾素-α、聚醚化干擾素-α、拉米夫定、阿德福韋酯、恩替卡韋、替比夫定、富馬酸替諾福韋二吡呋酯以及富馬酸替諾福韋艾拉酚胺。慢性B肝(CHB)可導致如肝硬化、肝細胞癌(HCC)等危機健康問題。
全球約有20%的慢性HBV感染者會發生肝硬化,隨後導致肝功能不全和門靜脈高壓。此外,全球相關領域臨床工作者還注意到,這部分CHB發生HCC風險要比非攜帶者高100倍。在眾多臨床試驗中,科學家主要觀察到,B肝e抗原陽性受試者發展為肝細胞癌風險最高。在肝硬化或肝癌晚期,肝移植已成為唯一選擇。
因此,早期發現HBV感染並及時治療至關重要。核苷(酸)類似物(NAs)一直以來被視為廣譜抗病毒藥物設計而展開積極研發。由於HBVDNA聚合酶是核苷或核苷(酸)類似物的主要靶點,因而該靶點開發設計方向也將圍繞此展開。目前,一些已用於治療HIV感染藥物的聯合使用,在未來也可能被用於治療HBV感染。
其他已報導的,針對B肝病毒複製周期,包括對B肝病毒DNA聚合酶或其他分子等,比如小干擾RNA(siRNAs)顯示出,siRNA可在體外抑製B肝病毒複製,在體內抑製以及相關分子抑製病毒核酸和病毒蛋白的表達。還有一些例如,抑製核衣殼形成;特異性抑製HBV表面抗原分泌等其結構作用模型有待闡明,部分小分子化合物的臨床前模型,均表現出較高抗病毒活性和安全性。

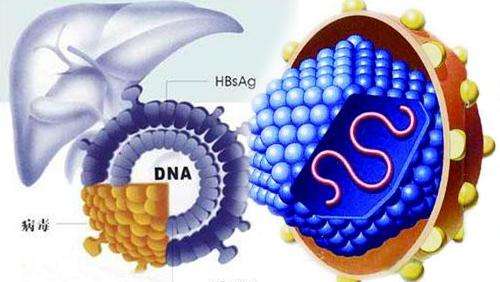
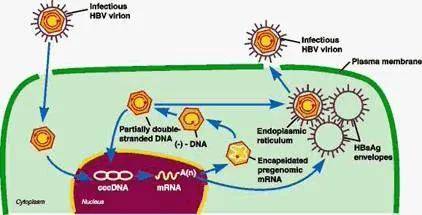
總體來看,全球B肝創新藥不同靶點均圍繞B肝病毒複製周期的不同步驟展開設計。B肝病毒複製模板,共價閉合環狀DNA(cccDNA)曾經在大量文獻期刊中被論證,其可能預示著肝細胞癌發展風險。全球有科學家也曾經進一步證明,腫瘤組織中cccDNA水準高於非腫瘤組織。病毒體包含一個3.2kb的松弛圓形(RC)DNA,有4個重疊的orf,即P、C、S和X。
S基因編碼3種表面蛋白:大、中、小HBsAg。聚合酶是由P ORF翻譯而來。聚合酶蛋白由4個結構域組成,它們分別是末端蛋白、間隔區、RT和RNase H。在RT的7個亞結構中,C結構域包括高度保守的TMDD基序,即酶的催化位點。感染肝細胞也含有B肝核心抗原(HBcAg)。HBcAg是由ORF C結構域編碼的B肝e抗原(HBeAg)。

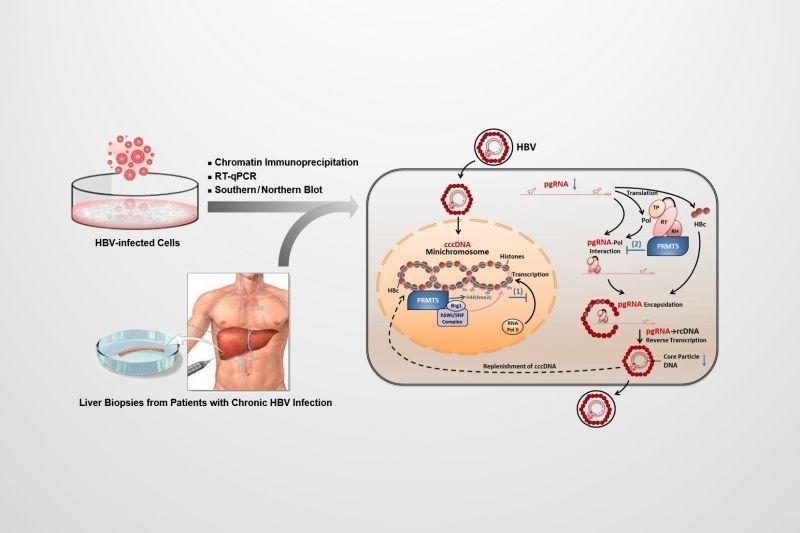
在與未知的受體相互作用後,病毒粒子的RC DNA被運送到細胞核,並轉化為共價閉合環狀DNA(cccDNA),而核衣殼則留在細胞質中。這種DNA中間體在病毒持久性中起著重要作用,並作為宿主RNA聚合酶II的轉錄模板,產生4個mRNA轉錄本。正如上面提到的,cccDNA在預測HCC以及開發新藥方向都有相當意義,但目前為止,基於cccDNA的化合物主要為抑製劑,科學界暫未尋找到清除cccDNA化合物。返回搜狐,查看更多
責任編輯: