雷莫蘆單抗獲批,看肝癌二線治療如何布局?
在全球範圍內,肝癌是癌症相關死亡的主要原因之一。在美國,肝癌是少數幾個發病率每年持續上升的主要癌症之一,也是癌症死亡上升最快的原因。
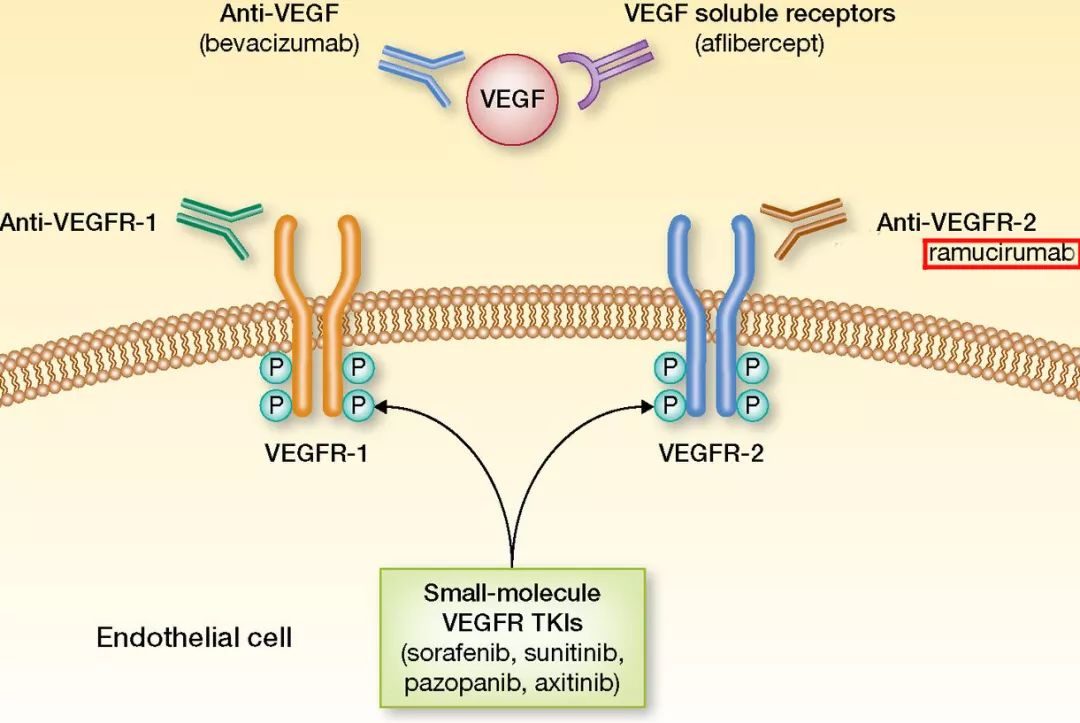
日前,美國食品和藥物管理局(FDA)宣布已批準ramucirumab(雷莫蘆單抗)作為一種單葯療法二線治療甲胎蛋白(AFP)≥400ng/ ML且之前已接受過索拉非尼治療的肝細胞癌患者。
該批準是基於國際,雙盲,安慰劑對照,多中心III期REACH-2試驗的結果,其中雷莫蘆單抗的中位總生存期(OS)為8.5個月,而安慰劑組為7.3個月(HR=0.71; 95%CI,0.53-0.95,P = .020)。
REACH-2試驗是在REACH試驗基礎上開展的,REACH試驗是針對索拉非尼治療失敗的肝癌病人,對比雷莫蘆單抗與安慰劑之間二線治療療效差異,但該試驗沒有獲得預期的結果。未選擇人群的中位OS雷莫蘆單抗組為9.2個月,而安慰劑組為7.6個月(HR,0.87; 95%CI,0.72-1.05; P = .14 ),無統計學意義。
但是其亞組分析顯示,AFP(甲胎蛋白)超過400ng/ml的患者可以從雷莫蘆單抗的治療中獲益。基線AFP≥400ng/ mL患者的中位OS在雷莫蘆單抗組為7.8個月,而安慰劑組為4.2個月(HR,0.674; 95%CI,0.51- 0.90; P = .0059)。相比之下,基線AFP <400 ng / mL的患者,雷莫蘆單抗組的中位OS為10.1個月,而安慰劑組為11.8個月。
由此開展了REACH-2試驗,結果發現,與安慰劑相比,雷莫蘆單抗無論在總生存還是無進展生存時間上都為患者帶來了獲益。
研究方法
REACH-2試驗於2015年開始,在全球20個國家共招募了292名患者,是首個在通過生物標誌物檢測分類的患者群體中進行的3期HCC試驗。
入組標準包括:≥18歲;組織學或細胞學確診為肝細胞癌HCC;巴塞隆納臨床肝癌(BCLC)分期B期或C期;Child-Pugh評分為A;AFP≥400ng/ mL,先前隻接受過索拉非尼治療。
入組患者按2:1隨機分組接受雷莫蘆單抗靜脈注射(IV)8 mg / kg,加上最佳支持治療或安慰劑/最佳支持治療,每2周一次,直至疾病進展或出現不可耐受的毒性。主要終點是OS。次要終點包括無進展生存(PFS),進展時間,緩解率,癥狀惡化時間和安全性。
研究結果
292名患者(雷莫蘆單抗組:n = 197 安慰劑組:n = 95)中位年齡為64歲,男性約佔研究人群的80%。大多數患者的Child-Pugh評分為A-5,超過80%的患者BCLC C期,並且約三分之二的患者病因為乙型或丙型肝炎。
?中位隨訪時間為7.9個月,數據顯示雷莫蘆單抗組中位OS顯著長於安慰劑組,分別為8.5個月 vs 7.3個月(HR= 0.710,P=0.0199),達到了研究的主要終點。
?與安慰劑組相比,雷莫蘆單抗組PFS也取得了統計學意義的顯著改善(中位PFS:2.8個月[95%CI:2.8-4.1] vs 1.6個月[95%CI:0.34-0.60],HR=0.45,95%CI:0.34-0.60,p<0.0001),達到了研究的次要終點。
?雷莫蘆單抗組客觀緩解率(ORR)高於安慰劑組(4.6% vs 1.1%,p=0.1697)。
?同時,雷莫蘆單抗組的疾病控制率也顯著高於安慰劑組,分別為59.9%和38.9%(P = .0006)。
安全性方面,雷莫蘆單抗雖然治療相關的不良事件(AEs)更多,但通常耐受性良好。雷莫蘆單抗最常報告的≥3級AE是高血壓(12.2%),腹水(4.1%)和疲勞(3.6%)。此外,雷莫蘆單抗中10.7%的患者因AEs而停止治療。雷莫蘆單抗組中有三分之一的患者需要調整劑量來控制治療相關的AE。
小結
肝癌的二線治療已經邁入了新的階段,一線治療耐葯後無葯可用的時代已經過去了。
?2017年4月,FDA批準瑞戈非尼用於索拉非尼耐葯肝癌的二線治療;
?2017年9月,FDA批準納武單抗用於索拉非尼耐葯肝癌的二線治療;
?2018年11月,FDA批準派姆單抗用於索拉非尼耐葯肝癌的二線治療;
?2019年1月,FDA批準卡博替尼用於索拉非尼耐葯肝癌的二線治療;
?2019年5月,FDA批準雷莫蘆單抗用於索拉非尼耐葯肝癌的二線治療。
2019版CSCO肝癌指南如下推薦:


ai幫幫
文章來源:ai幫幫平台
參考文獻:
1.FDA Approves Ramucirumab for Hepatocellular Carcinoma. FDA. Published May 10, 2019. https://bit.ly/2HeWrD7. Accessed May 10, 2019.
2.Zhu AX, Kang Y-K, Yen C-J, et al. REACH-2: A randomized, double-blind, placebo-controlled phase 3 study of ramucirumab versus placebo as second-line treatment in patients with advanced hepatocellular carcinoma (HCC) and elevated baseline alpha-fetoprotein (AFP) following first-line sorafenib. J Clin Oncol. 2018;36 (suppl; abstr 4003).
3.Zhu AX, Ryoo B-Y, Yen C-J, et al. Ramucirumab (RAM) as second-line treatment in patients (pts) with advanced hepatocellular carcinoma (HCC): analysis of patients with elevated α-fetoprotein (AFP) from the randomized phase III REACH study. Presented at: 2015 Gastrointestinal Cancers Symposium; January 15-17, 2015; San Francisco, CA. Abstract 232.
4.Zhu AX, Park JO, Ryoo B-Y, et al. Ramucirumab versus placebo as second-line treatment in patients with advanced hepatocellular carcinoma following first-line therapy with sorafenib (REACH): a randomised, double-blind, multicentre, phase 3 trial. Lancet Oncol. 2015; 16(7):859-870. doi: 10.1016/S1470-2045(15)00050-9.