狼瘡性腎炎是系統性紅斑狼瘡(SLE)最嚴重的表現之一,可顯著增加發病率和死亡率。既往研究證實狼瘡性腎炎患者20年腎臟生存率僅為68%。雖然糖皮質激素、環磷醯胺和其他免疫抑製劑的引入大大提高了狼瘡性腎炎患者的生存率,但仍有35%的狼瘡性腎炎患者會出現至少一次複發,5%-20%的患者進展為終末期腎病。
基於臨床前模型數據,自體造血乾細胞移植(簡稱自體乾細胞移植)已用於多種嚴重自身免疫性疾病(包括SLE)的治療,但其在狼瘡性腎炎中的應用研究較為有限。近期,劉志紅院士帶領團隊開展了一項研究,就自體造血乾細胞移植治療難治性狼瘡腎的有效性和安全性進行評估。該研究結果於5月7號發表於CJASN,為難治性狼瘡性腎炎患者提供了新型治療方案。
研究回顧
該研究共納入22名難治性狼瘡性腎炎患者,其中男性患者9名,女性患者13名,中位狼瘡性腎炎時間46(33-71)個月。難治性狼瘡性腎炎定義為:一種以上免疫抑製劑(包括糖皮質激素、環磷醯胺、他克莫司、霉酚酸酯和環孢素)治療6個月無應答或維持治療期複發,腎臟病理改變或抗體持續陽性。其他納入標準為年齡14-45歲,血肌酐<2 mg/dl,丙氨酸轉氨酶相比正常上限值小2倍,左心室射血分數>50%,無活動性感染。
外周血白細胞<1×109/L時給予環磷醯胺(2.0g/m2,2天)聯合粒細胞集落刺激因子(G-CSF,5-10 mg/kg/d)動員外周造血乾細胞。監測外周血白細胞計數,當出現反彈時進行收集(一般在使用環磷醯胺後11天)。
移植前預處理方案為:移植前5天靜脈注射環磷醯胺(40mg/kg/d ×4d),總劑量為160mg/kg;移植前4天注射兔抗人胸腺細胞免疫球蛋白(ATG,2.5mg/kg/d ×3d)。根據患者病情可減少環磷醯胺和ATG劑量。使用ATG的同時輸注甲潑尼龍(80-500 mg/d)以減少過敏反應。輸注乾細胞後第二天給予G-CSF(0.5 mg/kg/d),直至外周血白細胞絕對計數持續>1×109/L。
中位隨訪時間為72(60-80)個月。主要終點為患者緩解率,包括完全緩解(蛋白尿<0.4 g/24h,紅細胞<3個/高倍視野,血清白蛋白>3.5 g/dl,血肌酐<1.24 mg/dl)、部分緩解(蛋白尿降低≥50%,尿蛋白排泄量<3.5 g/dl,血清白蛋白>30 g/L,血肌酐<1.24 mg/dl)和無緩解(未獲得部分緩解)。次要終點為生存率、複發率,蛋白尿變化,腎功能和血清免疫學檢查以及不良反應。
主要發現
所有患者均成功移植,粒細胞和血小板移植中位時間分別為8(7-9)和9(6-10)天。
自體乾細胞移植後C3顯著增加(P<0.05),移植後3個月中位C3水準從0.55(0.44-0.70)增至0.98(0.84-1.12)g/L(圖1)。C4亦顯著增加,但無統計學意義。移植後ANA降低,SLE疾病活動度指數評分於移植後1個月即顯著降低,並維持在低水準(P<0.05)。
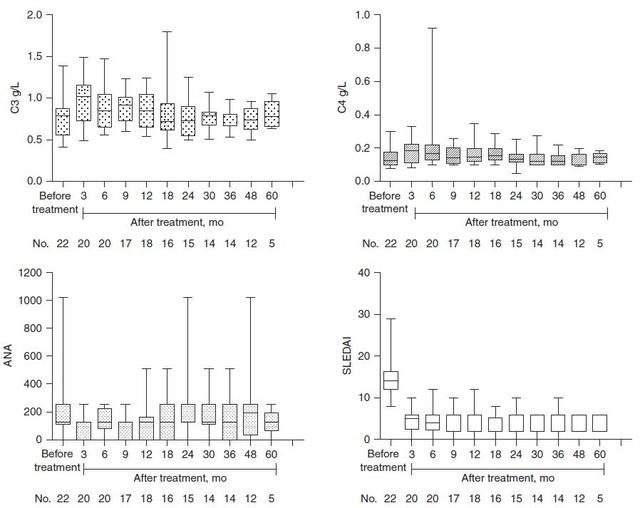

圖1 自體乾細胞移植後C3、C4、ANAs和SLE疾病活動度指數評分改善
隨訪期間平均蛋白尿為<0.5g/24h,平均血清白蛋白>4.5g/dl(圖2)。


圖2 自體乾細胞移植後蛋白尿和血清白蛋白改善
隨訪結束,共18例(82%)患者獲得完全緩解,完全緩解中位時間為3個月(圖3A)。1例(5%)患者獲得部分緩解,1例患者無應答並在移植後12個月行腹膜透析。5年腎臟總生存率為86%(圖3B)。6例患者出現複發,複發率為27%,中位複發時間為31(13.5-55)個月,5年無複發生存率為53%(圖3C)。


圖3 A:完全緩解率,B:腎臟生存率,C:複發率,D:總生存率
隨訪期間共2名患者死亡,1例患者在移植後1個月死亡嚴重感染,1例患者在移植後5個月死於肺部感染。移植相關相關死亡率為5%(1例)。總生存率為91%(圖3D)。
乾細胞移植的主要併發症是高熱和胃腸道癥狀(表1)。
表1 移植相關不良反應


隨訪期間最常見的併發症為感染,主要發生於移植後6個月內(表2)。其他併發症包括純紅細胞再生障礙性貧血、白細胞減少症和血小板減少症。
表2 隨訪期間併發症


小結
該研究顯示,自體乾細胞移植患者大多數(82%)獲得完全緩解,腎臟應答中位時間僅為3個月。隨訪結束後5年總生存率和無病生存率為91%和53%。自體造血乾細胞移植相對安全且預後良好,可作為難治性狼瘡性腎炎的治療選擇。
醫脈通編譯自:Autologous Hematopoietic Stem Cell Transplantation for Refractory Lupus Nephritis. CJASN. May 2019, 14 (5) 719-727.







