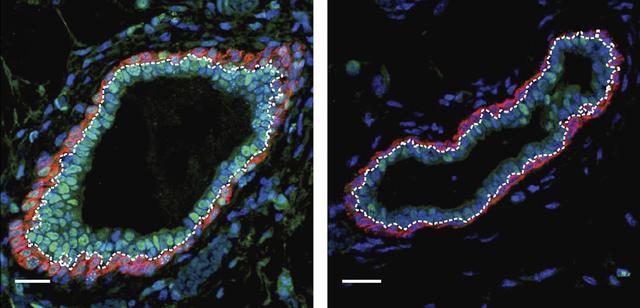
11 月 20 日,Nature Communications 發表了一項最新研究,波士頓兒童醫院的研究人員發現,一種看起來很有希望用於肺癌的表觀遺傳療法實際上具有相反的效果,可以增強被認為可以驅動腫瘤的癌症乾細胞。
研究人員表示,他們發現了表觀遺傳治療可能會增加肺癌乾細胞的發展,同時增加了腫瘤乾細胞對癌症發展驅動的證據。研究人員也基於此提出了癌症治療的新策略。
(圖片來源:genengnews.com)
表觀遺傳學是指在基因組序列不變的情況下,基因表達發生了可遺傳的變化,並最終導致了表型的變化。這些表觀遺傳學變化包括 DNA 的甲基化修飾、組蛋白的各種修飾等。
過去十年來對人類癌症基因組的綜合分析顯示,在許多癌症中參與基因表達,DNA 修復和 DNA 複製的表觀遺傳調控蛋白都出現了突變。組蛋白突變可以阻礙細胞分化,促進惡性腫瘤發展。這些發現表明表觀遺傳調節失控在癌症的發生和進展中起了關鍵作用。
因此,靶向控制基因開關酶的表觀遺傳療法,在癌症治療領域越來越受到關注。
在這項研究中,研究人員對一種抑製 G9a 酶(一種組蛋白甲基轉移酶)的表觀遺傳療法進行研究。近年來的研究表明,組蛋白甲基化轉移酶 G9a 調控自噬反應和細胞分化,在腫瘤發生過程中起著重要作用。
在一般的腫瘤細胞實驗中,靶向 G9a 的抑製藥物會減緩癌細胞生長甚至殺死癌細胞,但是研究人員這次卻發現,抑製 G9a 酶的藥物卻使得存活的腫瘤細胞更像腫瘤乾細胞,並進一步促進腫瘤的發展。

(圖片來源:trialsitenews.com)
腫瘤乾細胞是腫瘤的一部分,可以自行再生腫瘤。腫瘤乾細胞對腫瘤的存活、增殖、轉移及複發有著重要作用。從本質上講,腫瘤乾細胞通過自我更新和無限增殖維持著腫瘤細胞群的生命力。目前已經在血癌和多種實體瘤中鑒定出腫瘤乾細胞。
研究論文第一作者 Rowbotham 表示,「人們研究了肺部腫瘤的細胞系,發現他們對於靶向 G9a 的抑製藥物很敏感,但我們發現這些藥物會使得腫瘤細胞更像乾細胞,這是我們看到的現象。」
波士頓兒童醫院乾細胞研究項目的 Carla Kim 博士及其同事也已經證明,腫瘤乾細胞在最常見的肺癌類型腺癌中發揮關鍵作用。當他們從肺癌小鼠中將腫瘤乾細胞移植到正常小鼠體內時,能夠導致健康小鼠的癌症發生。
Kim 表示,「早期的研究可能因為腫瘤乾細胞難以檢測,G9a 的這一不利因素並未引起注意。當你用這些藥物治療時,腫瘤乾細胞就更多,因為它們只是腫瘤的一小部分,任何影響它們的因素都很容易被遺漏。」
但研究人員同時也發現了一個可能更好的靶標:組蛋白去甲基化酶。與組蛋白甲基化轉移酶不同,去甲基化酶的作用是從組蛋白中去除甲基。據此研究人員還確定了一種減少腫瘤乾細胞細胞,抑製小鼠肺癌的策略。

圖 | 組蛋白甲基化(圖片來源:epigentek.com)
當研究人員給具有確定肺腫瘤的小鼠提供去甲基化酶抑製劑時,癌症進展減慢並且比未治療的小鼠存活更長時間。
儘管尚未在人類腺癌中發現腫瘤乾細胞,但 Kim 認為這一發現值得進一步研究。她指出了一個相關的證據,一項 2017 年的研究發現,去甲基酶抑製劑可有效殺死患者腫瘤中的化療耐葯細胞。
「即使我們無法確定人類患者的腫瘤乾細胞,這項研究工作也表明你可以從小鼠模型中研究腫瘤乾細胞,並找出可能具有臨床重要性的靶點,」Kim 說,「它顯示了尋找癌症敏感的正確分子的重要性。在腺癌中,去甲基酶抑製劑比甲基轉移酶抑製劑更有用。」
研究人員也因此設想了一種針對肺腺癌的兩階段策略,該策略首先針對腫瘤中的一般癌細胞進行治療,然後添加專門針對癌症乾細胞的第二種治療。
該團隊正在進行進一步的研究,以探索去甲基酶抑製劑作為潛在治療藥物,單獨或與其他治療組合的價值。因為去甲基酶抑製劑具有非常廣泛的作用,它們還將尋找抑製劑對下遊基因的影響,這可以提供更具體的藥物靶標。