▎葯明康德/報導
日前,專註於開發創新單克隆抗體癌症療法的臨床階段生物醫藥公司MacroGenics宣布,其在研單抗藥物margetuximab,在治療轉移性人表皮生長因子受體2陽性(HER2+)乳腺癌的關鍵3期試驗SOPHIA中,取得了積極結果。MacroGenics計劃於2019年下半年為margetuximab提交生物製劑許可申請(BLA)。


約五分之一的乳腺癌和胃癌有過度表達的HER2,這是一種在某些侵襲性癌細胞表面發現的酪氨酸受體激酶。許多HER2+腫瘤進展後,一些現有的獲批療法已經無法繼續有效控制疾病。在接受曲妥珠單抗(trastuzumab)、帕妥珠單抗(pertuzumab)和Kadycla(trastuzumab emtansine)治療後,目前沒有獲批藥物對疾病繼續惡化的HER2+乳腺癌患者進行治療。
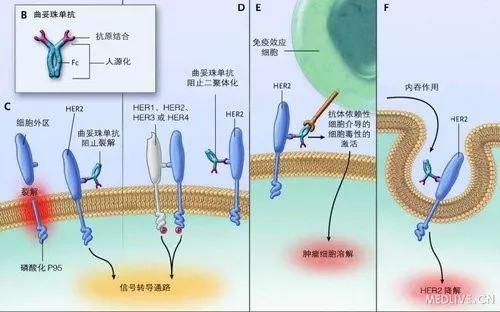
Margetuximab是MacroGenics公司研發的對抗體Fc端進行優化的HER2單克隆抗體。抗體Fc端通過與表達在免疫細胞表面的FcγRs受體結合,能夠引發多種免疫反應,例如抗體依賴性細胞介導的細胞毒作用(antibody-dependent cellular cytotoxicity,ADCC)。MacroGenics利用其專有的Fc優化技術平台增加了margetuximab對激活性FcγRs受體的親和力,進而能增強抗體藥物與免疫效應細胞之間的相互作用,從而提高細胞的效應功能。
共有536名患者參與的SOPHIA試驗,旨在評估margetuximab和化療構成的組合療法,與曲妥珠單抗和化療構成的組合療法相比,治療轉移性HER2+乳腺癌患者的有效性,耐受性和安全性。所有的試驗對象都曾經接受過HER2+乳腺癌常用療法的治療,其中90%的患者接受過trastuzumab emtansine的治療。
Margetuximab達到了試驗的主要終點,與對照組相比,延長了患者的無進展生存期(PFS),降低疾病進展風險24%(HR=0.76, p=0.033)。在攜帶FcγRs 158F變異的預先指定亞組,margetuximab與化療構成的組合療法與對照組相比,降低疾病進展風險32%(HR=0.68, p=0.005)。攜帶FcγRs 158F變異的患者通常對曲妥珠單抗的響應不良。


▲MacroGenics的產品研發管線(圖片來源:MacroGenics官網)
MacroGenics總裁兼首席執行官Scott Koenig博士說:「MacroGenics對SOPHIA試驗的結果非常滿意,並在這裡對所有參與試驗的患者及其家人,研究人員們表示深深的感謝。MacroGenics通過優化Fc結構域增強免疫反應的抗體分子,與常用HER2+乳腺癌療法相比,展示了其優越的療效。我們期待進一步驗證margetuximab對其它HER2+乳腺癌和HER2+胃癌的療效。」
參考資料:
[1] MacroGenics Announces Positive Results from Pivotal Phase 3 SOPHIA Study of Margetuximab. Retrieved Feb. 6, 2019, from https://globenewswire.com/news-release/2019/02/06/1711231/0/en/MacroGenics-Announces-Positive-Results-from-Pivotal-Phase-3-SOPHIA-Study-of-Margetuximab.html
[2] ASCO | 靶向HER2,乳腺癌創新ADC療法緩解率超50%!. Retrieved Feb. 6, 2019, from https://mp.weixin.qq.com/s/kLa9W3fbjKl9HMTveY3e_w
本文來自葯明康德微信團隊,歡迎轉發到朋友圈,謝絕轉載到其他平台;如有開設白名單需求,請在文章底部留言;如有其他合作需求,請聯繫[email protected]