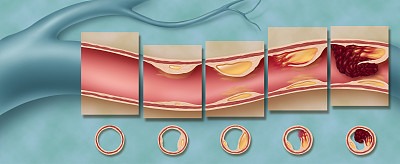
隨著2018年美國心臟病學會/美國心臟協會(ACC/AHA)膽固醇管理指南的發布,大家對血脂和風險因素個體化管理的熱情日益高漲。有幾種降脂葯,如他汀類藥物、依折麥布和PCSK9抑製劑,已證明可降低動脈粥樣硬化性心血管疾病(ASCVD)的風險。他汀類藥物經歷了一次重大的範式轉變,從最初用於降低家族性高膽固醇血症(FH)患者的低密度脂蛋白膽固醇(LDL-C),到調節一般人群的ASCVD風險和一級預防。
醫脈通編譯整理,未經授權請勿轉載。
幾乎三分之一的美國人服用他汀類藥物;然而,高達15%的患者報告他們對第一次處方的他汀類藥物不耐受。此外,大約一半被處方他汀類藥物的患者在使用兩年後LDL-C的降低幅度並不理想(> 40%)。在許多患者中,儘管改善了生活方式並使用這些藥物進行治療,但ASCVD風險仍然居高不下。因此必須研究新的治療方法,以減少心血管殘餘風險。本文重點介紹除PCSK9抑製劑以外的新型降脂藥物。
FH患者的早發CVD風險較高。FH可以通過多種機制進行乾預。目前,國際動脈粥樣硬化學會(IAS)指南建議,改善生活方式和飲食,同時使用高強度他汀類藥物+依折麥布作為一線治療方案。在雜合子FH患者中,他汀類藥物單葯治療已被證明可降低44%的冠狀動脈疾病(CAD)和死亡風險。其他研究已經證實,大劑量他汀類藥物聯合依折麥布可減少這些患者的心血管事件。如果LDL-C未達標或降低<50%,根據IAS指南,基於費用和可用性,加用煙酸、膽汁酸螯合劑或PCSK-9抑製劑。值得注意的是,這些建議與ACC/AHA指南有衝突,在ACC/AHA指南中,PCSK9抑製劑要優於煙酸或膽汁酸螯合劑。據報導,在使用他汀類藥物聯合PCSK9抑製劑治療的FH患者中,80%患者的LDL-C達標。如果LDL-C仍未達標或降低<50%,則可考慮進行血漿分離(apheresis),使用洛美他派(lomitapide)或米泊美生(mipomersen)。
洛美他派是微粒體甘油三酯轉運蛋白(MTP)的抑製劑,MTP負責組裝含有apoB的脂蛋白。 MTP抑製劑可降低缺乏功能性LDL受體的FH患者的apoB水準。米泊美生是一種與apoB mRNA互補的反義寡核苷酸,從而抑製apo-B100,也用於FH的治療。ATP檸檬酸裂解酶(ACL)在膽固醇合成中起作用,抑製ACL可減少膽固醇合成。新型藥物Bempedoic acid通過抑製ACL和激活AMP來降低LDL-C。基因治療法也正在開發中。
表1 新型降脂藥物
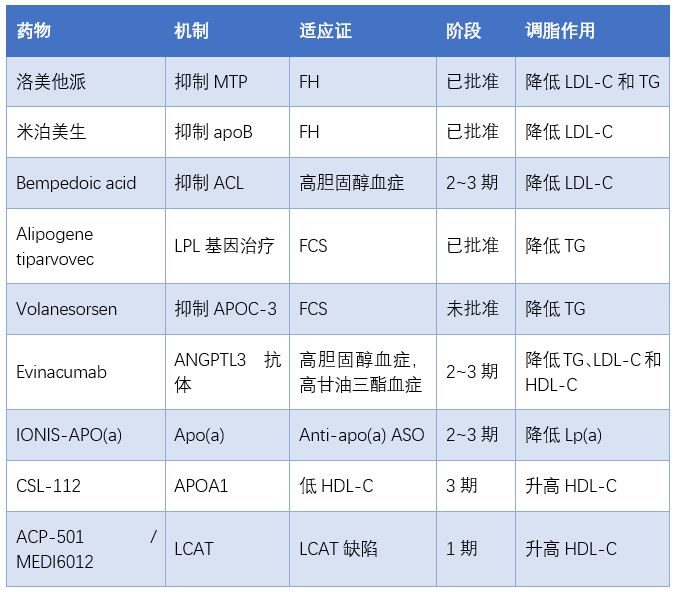
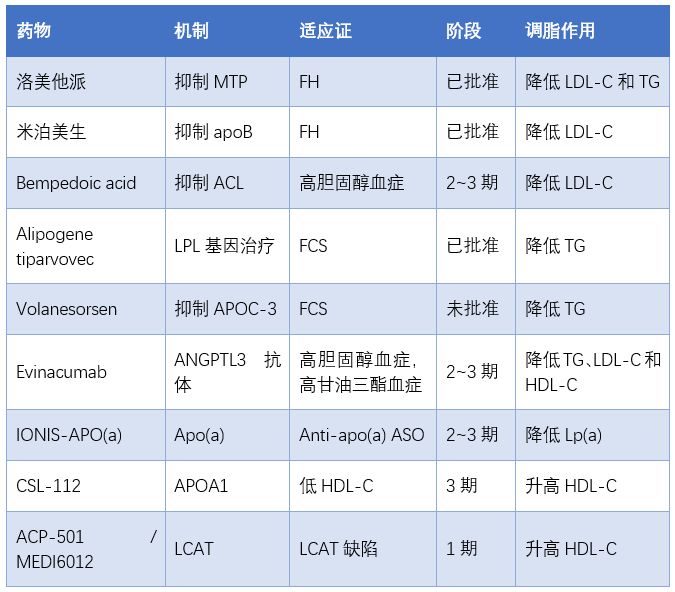
註:ACL ,ATP檸檬酸裂解酶;FCS,家族性乳糜微粒血症綜合征;FH,家族性高膽固醇血症;LPL,脂蛋白脂酶;LCAT,卵磷脂膽固醇脂醯基轉移酶;MTP,微粒體甘油三酯轉運蛋白


圖1 新型降脂藥物的機制
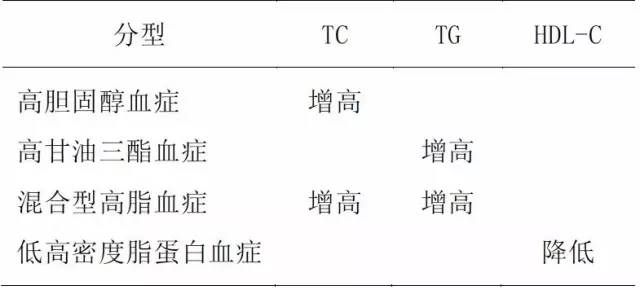
甘油三酯(TG)也與ASCVD風險有關。然而,有人認為TG本身並不直接導致斑塊形成,而是極低密度脂蛋白(VLDL)顆粒、殘餘物和中間密度脂蛋白(IDL)在斑塊形成中發揮了最強作用。TG和殘餘顆粒相互作用,增加動脈粥樣硬化形成。高甘油三酯血症既可能源於單基因疾病(家族性乳糜微粒血症綜合征,FCS),也可能是繼發性表現。繼發性高甘油三酯血症患者的ASCVD風險似乎比單基因乳糜微粒血症更高。他汀類藥物已被用於治療高甘油三酯血症,煙酸、貝特類和omega-3脂肪酸被推薦用於治療高甘油三酯血症。
REDUCE-IT研究顯示,Vascepa(高劑量二十碳五烯酸乙酯,ω-3脂肪酸)可降低患有CVD或有CVD風險,以及使用他汀類藥物且LDL-C控制良好的患者的甘油三酯水準及心血管事件和死亡風險。使用Vascepa和使用安慰劑患者的主要複合終點發生率分別為17.2%和22%,絕對風險降低了4.8%。有幾種用於治療高甘油三酯血症的新葯已經進行了試驗,包括載脂蛋白C-III(apo C-III)抑製劑和脂蛋白脂酶(LPL)基因治療(圖1)。Apo C-III存在於乳糜微粒和VLDL上,通過抑製LPL活性來干擾甘油三酯的清除。
Volanesorsen是一種反義寡核苷酸,可抑製Apo-CIII mRNA的翻譯,從而降低甘油三酯。由於有一定的血小板減少症風險,Volanesorsen用於FCS和難治性高甘油三酯血症未能獲得FDA的最終批準。高甘油三酯血症的其他靶點包括apoCII、apoA-V和ANGPTL4。
雖然HDL-C是心血管事件風險的反向預測因子,但人類遺傳學研究未能顯示HDL-C和ASCVD風險之間存在類似於LDL的因果關係。換句話說,沒有證據表明在人類中提高HDL-C可以降低ASCVD事件的風險。
膽固醇酯轉運蛋白(CETP)可以將膽固醇酯從非致動脈粥樣硬化的HDL轉移至潛在致動脈粥樣硬化的非HDL。雖然早期研究顯示CETP缺乏與高HDL-C水準和ASCVD預防相關,但後來的研究結果並不樂觀。三種不同的CETP抑製劑均未能減少大型隨機臨床試驗中的ASCVD事件,這使HDL假說受到了質疑。其中一種可能性是HDL功能可能與ASCVD風險評估更相關。
ApoA-I是另一種與HDL功能相關的蛋白,存在於HDL和乳糜微粒上。基於動物模型,猜測輸注ApoA-I可能起到穩定斑塊和調節動脈粥樣硬化消退的作用。在過去幾年中,一些HDL模擬物已經進入臨床試驗階段。從初步結果來看,用這些藥物治療未能對主要療效終點產生顯著影響。然而,這可能更適合家族性低脂蛋白血症(FHA)和純合子FH患者,小規模研究正在進行中。
大多數新型脂質療法都來自於對具有嚴重表型的罕見病的研究,孟德爾隨機化心血管結局研究可以有效地驗證治療靶點。雖然新的生物製劑和靶向治療可能是某些患者未來的二線治療方案,但目前最有效的方法是通過改善生活方式和使用循證藥物來進行最大程度的預防。
醫脈通編譯自:Personalizing Lipid Targets – Beyond PCSK9 Inhibitors. ACC. Jul 16, 2019.