法制晚報·看法新聞(記者 黎史翔)繼6月15日獲國家藥品監督管理局批準後,歐狄沃(納武利尤單抗注射液)將於今年第三季度正式登陸中國市場,滿足肺癌患者的治療需求。法制晚報·看法新聞記者了解到,該葯是中國首個獲批上市的免疫腫瘤治療藥物。
獲批上市
有望填補國內免疫腫瘤治療空白
據了解,這款由美國製藥公司百時美施貴寶生產的新藥用於治療表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、既往接受過含鉑方案化療後疾病進展或不可耐受的局部晚期或轉移性非小細胞肺癌(NSCLC)成人患者。
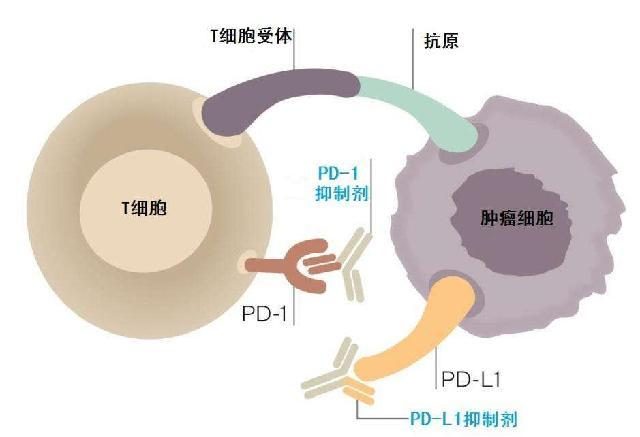
PD-1 (程式性死亡受體1)藥物在國內的首次獲批上市即被業界被稱為 「歡欣鼓舞 」,「抗癌神葯」帶來的是全新的抗腫瘤理念。
廣東省人民醫院終身主任、中國胸部腫瘤研究協作組主席吳一龍教授表示:「與傳統治療方式不同,免疫腫瘤治療並不直接作用於腫瘤本身,而是通過激活患者自身的免疫系統來抗擊腫瘤,具有毒副作用小、療效持久等特點。」吳一龍教授表示,「作為國內首個獲批上市的免疫腫瘤(I-O)治療藥物,歐狄沃為醫生及患者提供了全新的治療選擇,在中國有望成為非小細胞肺癌二線治療的新標準。」
他稱,「在全球大多數國家和地區,歐狄沃已成為二線非小細胞肺癌的標準治療。作為中國目前唯一獲批用於肺癌治療的PD-1抑製劑,歐狄沃的上市毋庸置疑將成為中國癌症治療領域的裡程碑,有望填補國內免疫腫瘤治療的空白,為更多中國晚期非小細胞肺癌患者帶來長期生存的希望。」
審批快車道
從提交申請到獲批僅用了7個月
數據顯示,肺癌的發病率和死亡率一直高居所有癌症之首 ,是中國公共衛生領域刻不容緩的議題。由於肺癌早期癥狀較為隱匿,大多數患者在確診時已為晚期。近年來,儘管肺癌在治療手段上不斷推陳出新,但對於晚期無驅動基因突變的患者而言,目前的治療仍以化療為主,總體預後較差,改善治療現狀、獲得長期生存是晚期肺癌患者最迫切的需求。
目前,肺癌仍然是中國一個重要的公共衛生議題。《「健康中國2030」規劃綱要》明確指出,到2030年,總體癌症5年生存率要提高15%。因此,改善患者治療現狀、提高創新藥物的可及性是社會各界共同努力的方向。
「要實現『健康中國2030』的目標,做好肺癌這一中國第一癌症的防治工作顯得尤為重要。我們既要促進創新藥物的可及,同時也需要切實提升創新服務的可及,通過探索創新性的醫療模式,真正做到以患者為中心。」 吳一龍教授表示。
事實上,自2015年藥品審評審批制度改革以來,新葯上市速度已在加快。記者了解到,歐狄沃從2017年11月提交上市申請到今年6月獲批,僅用了7個月的時間,預計今年第三季度登陸中國市場。
定價問題
響應各級醫保談判等方式 促進新葯在中國的可及性
目前百時美施貴寶還沒有公布「歐狄沃」在國內的定價。按照在美國的收費標準,使用歐狄沃的治療成本高昂。根據美國食品藥品監督管理局(FDA)在2016年9月批準修改後的歐狄沃的給藥方案,非小細胞肺癌患者按照「每2周1次,每次240mg」給葯,直至疾病進展或出現不可耐受毒性。歐狄沃240mg規格在美國的定價大約是6500美元,不考慮商業保險的因素,治療一年的成本大約為16.9萬美元(按目前匯率換算大約115.7萬元人民幣)。國外臨床上一般連續使用兩年後停葯。
有媒體報導分析指出,由於目前多家跨國葯企和中國本土企業都在研發PD-1藥物,除了百時美施貴寶,還有四家的產品也進入了國家葯監局的優先審評通道。因此市場留給歐狄沃一家的時間並不多,企業在PD-1藥物賽道上的競速或將促使歐狄沃採取更「親民」的定價策略。
關於該抗癌新葯在中國上市後如何定價。百時美施貴寶中國大陸及香港地區總裁趙萍女士在10日舉辦的媒體溝通會上表示,定價時會考慮患者的支付能力等多個因素,到時候會呈現一個滿意的定價。
趙萍稱,「百時美施貴寶將關注中國最迫切且未被滿足的治療領域,除肺癌之外,我們還將致力於探索免疫腫瘤(I-O)治療在包括肝癌、胃癌、食管癌等在內的不同高發瘤種中的應用,以期將創新的免疫腫瘤(I-O)治療藥物儘早帶給更多的中國患者。與此同時,我們將與各方攜手,通過實施多元化的舉措、響應各級醫保談判等方式,共同促進歐狄沃在中國的可及性,幫助中國晚期非小細胞肺癌患者改善治療現狀。」
法制晚報·看法新聞原創作品拒絕任何形式刪改,看法新聞保留追究法律責任的權利。