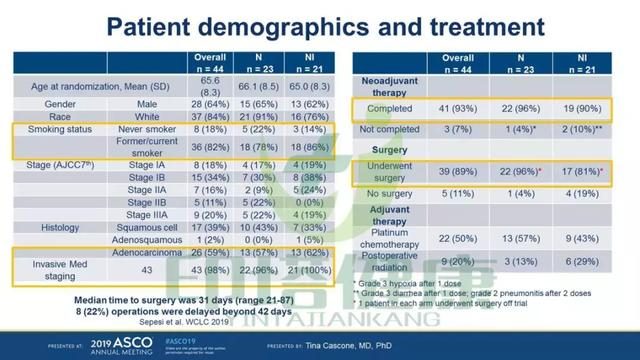
CheckMate 040是一項正在進行中的開放標籤、多隊列、1/2期臨床研究,旨在評估O葯或者以O葯為基礎的聯合治療方案對晚期肝癌患者的療效與安全性。該研究共包含6個隊列。其中,隊列1和隊列2是O葯的劑量爬坡與劑量擴展試驗。
2019年ASCO年會上公布了隊列4的研究數據,該隊列探索性地評估了三種不同劑量的O葯和Y葯聯合給藥方案的安全性和有效性。
臨床數據
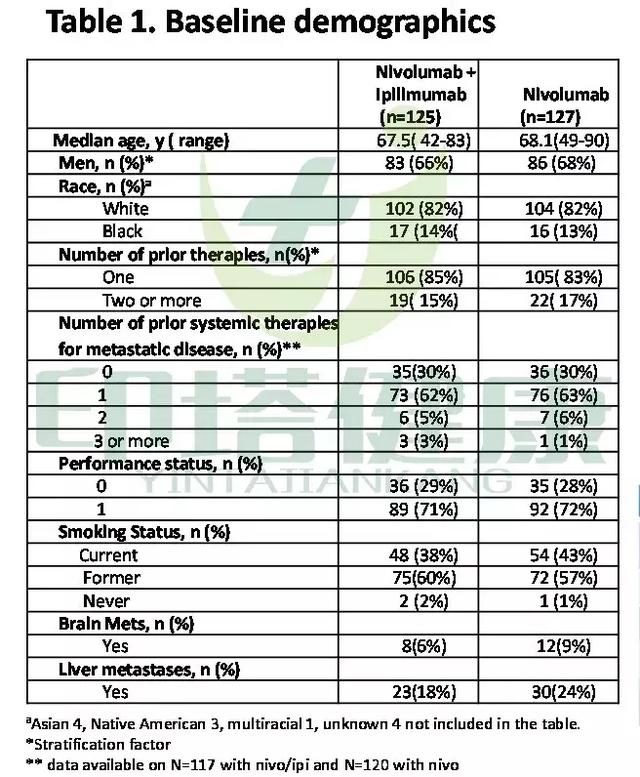
試驗共入組148名對索拉菲尼不耐受或接受索拉菲尼後有疾病進展的肝癌晚期患者,患者隨機分為3組,分別接受治療:
A組:患者每3周接受一次O葯+Y葯,O葯每次1mg/kg,Y葯每次3mg/kg,連續治療4個周期,之後每2周接受一次O葯,每次240mg;
B組:患者每3周接受一次O葯+Y葯,O葯每次3mg/kg,Y葯每次1mg/kg,連續治療4個周期,之後每2周接受一次O葯,每次240mg;
C組:患者每2周接受一次O葯,每次3mg/kg,每6周接受一次Y葯,每次1mg/kg。
持續治療直到疾病進展或出現不可耐受的毒性反應。
本次試驗的主要觀察終點為客觀反應率(ORR)和持續反應時間(DOR),次要觀察終點為疾病緩解率(DCR)、無進展生存期(PFS)、總生存期(OS)、反應時間(TTR)和疾病進展時間(TTP)。
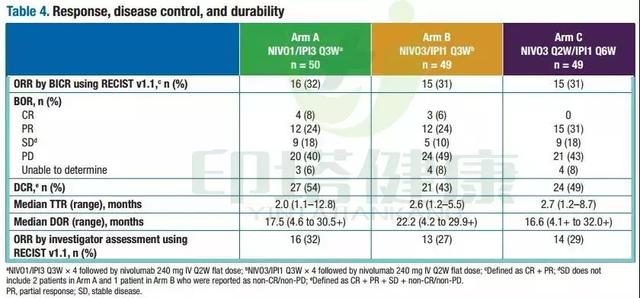
試驗結果表明,3組患者(A組 VS B組 VS C組)中,由盲法獨立審查委員會(BICR)評估的ORR為32% VS 31% VS 31%,CR為8% VS 6% VS 0%,PR為24% VS 24% VS 31%,SD為18% VS 10% 18%;由研究者評估的ORR為32% VS 27% VS 29%。
3組患者(A組 VS B組 VS C組)的DCR為54% VS 43% VS 49%,中位TTR為2個月 VS 2.6個月 VS 2.7個月,中位DOR為17.5個月 VS 22.2個月 VS 16.6個月。
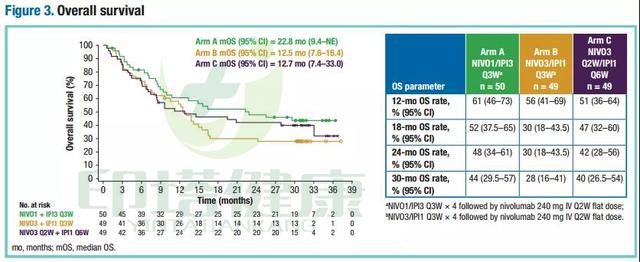
3組患者(A組 VS B組 VS C組)的中位OS為22.8個月 VS 12.5個月 VS 12.7個月。3組患者中,達到12個月OS的患者比例為61% VS 56% VS 51%,達到18個月OS的患者比例為52% VS 30% VS 47%,達到24個月OS的患者比例為48% VS 30% VS 42%,達到30個月OS的患者比例為44% VS 28% VS 40%。
PD-L1<1%的3組患者(A組 VS B組 VS C組)的ORR為31% VS 32% VS 28%,PD-L1≥1%的3組患者的ORR為30% VS 30% VS 50%。
PD-L1<1%的3組患者(A組 VS B組 VS C組)的中位OS為22.2個月 VS 12.5個月 VS 10.4個月,PD-L1≥1%的3組患者的中位OS為18.8個月 VS 10.2個月 VS NE(not estimated 未評估)。

不良反應
各治療組中,A組、B組和C組的治療相關不良事件 (TRAEs) 發生率分別為94%、71%和79%。最常見的3-4級TRAEs包括瘙癢、皮疹、腹瀉、穀草轉氨酶升高和脂肪酶升高。
小結
此次試驗首次證實了納武利尤單抗(O葯)聯合伊匹木單抗(Y葯)能讓既往接受過索拉非尼治療的晚期肝癌患者顯著獲益:
1、客觀反應率 (ORR) 達31%,中位持續反應時間 (mDOR) 為17.5個月;
2、中位總生存期 (mOS) 達22.8個月,30個月總生存率高達44%;
3、無論PD-L1表達水準如何,所有治療組均觀察到客觀緩解。
【重要提示】本公號【全球好葯資訊】所有文章信息僅供參考,具體治療謹遵醫囑!