葯明康德/報導

圖片來源:123RF
試驗藥物:傑諾單抗注射液
首次公示:2019-03-08
試驗通俗題目:GB226治療失敗的PD-L1 陽性的複發或轉移性宮頸癌患者
試驗專業題目:評價傑諾單抗注射液(GB226)治療含鉑方案化療失敗的PD-L1 陽性的複發或轉移性宮頸癌患者的有效性及安全性的II 期臨床研究
目標入組人數:國內試驗:80人
| 1 | 年齡≥18 周歲; |
| 2 | 理解研究步驟和內容,並自願簽署書面知情同意書; |
| 3 | 組織學或細胞學確診的宮頸癌; |
| 4 | 複發或轉移性宮頸癌患者,接受過至少一線含鉑方案化療後進展或複發 (如果患者在接受含鉑方案新輔助或輔助化療期間或結束後6 個月內進展或複發的,則被視為已接受一線治療); |
| 5 | 按照 RECIST 1.1 標準,受試者必須有至少一個通過CT 或MRI 檢查的 可測量的靶病灶(最長徑≥10mm 的病灶,或者短徑≥15mm 的淋巴結); |
| 6 | 預期生存期≥3 個月; |
| 7 | ECOG 評分0-1 分; |
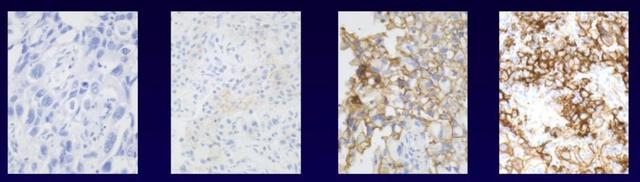
| 8 | 受試者需要提供足夠的且符合檢測標準的腫瘤存檔組織或新鮮組織製備的福爾馬林固定石蠟包埋(FFPE)標本或切片,並願意在需要時進行腫瘤組織活檢,用於PD-L1 的檢測。存檔組織必須是具有代表性的三年以內的腫瘤標本,或半年內新切的FFPE 腫瘤組織的未染色連續切 片(不少於4 片),還須提供上述標本的相關病理報告。新鮮組織標本的取材方式可接受手術切除術和活檢術。活檢的方式包括但不限於核心針頭活檢、內窺鏡下切除或鉗夾活檢術(需保證足夠的腫瘤細胞>100 個);不接受細針穿刺和液基細胞學檢測(TCT)樣本(即缺乏完整的組織結構僅提供細胞懸液和/或細胞塗片的樣本);不接受脫鈣的骨轉移腫瘤組織標本。對於針芯活檢標本,至少需提交3 針單個石蠟包埋的標本供評估。對於初始存檔腫瘤組織樣本中PD-L1 陰性的患者,在徵得患者同意後,可在篩選時進行活檢,以提供新鮮組織製備的蠟塊或切片重新檢測PD-L1 狀態,任何一種腫瘤組織樣本呈陽性結果,均符合本研究合格性; |
9
篩查所做的實驗室檢查的值必須符合下列標準:
血常規檢查(檢測前14 天內未輸血、未使用G-CSF、未使用藥物糾正): 1) 血紅蛋白(HGB)≥90 g/L; 2) 中性粒細胞絕對計數(ANC)≥1.5×10^9/L; 3) 血小板(PLT)≥100×10^9/L;
生化檢查 1) 總膽紅素(TBIL)≤1.5×正常值上限(ULN)(Gilbert 綜合征允許 ≤5×ULN); 2) 谷丙轉氨酶(ALT)和穀草轉氨酶(AST)≤2.5×ULN(如存在肝臟轉移,則ALT 和AST≤5×ULN); 3) 血清肌酐( Cr ) ≤ 1.5×ULN 或內生肌酐清除率≥ 50mL/min (Cockcroft-Gault 公式);
| 10 | 甲狀腺功能指標:促甲狀腺激素(TSH)、遊離甲狀腺素(FT3/FT4) 在正常範圍;若TSH 不在正常範圍的,FT3/FT4 在正常範圍可以入組; |
| 11 | 研究用藥前7 天內確認的未懷孕女性;生育期女性需同意在整個研究期 間及研究結束後6 個月內採取醫學上認可的有效避孕措施; |
| 12 | 受試者可以按期隨訪,能夠與研究者作良好的溝通並能夠依照本研究規 定完成研究; |
排除標準:
| 1 | 既往患有其他惡性腫瘤(已治癒的皮膚基底細胞癌或鱗狀上皮細胞癌除 外)的患者,不得參加本研究,除非她在入組前完全緩解至少5 年,並 且預估在整個研究期間不需要再接受其他抗腫瘤治療; |
| 2 | 活動性中樞神經系統(CNS)轉移,包括有癥狀的腦轉移或腦膜轉移或 脊髓壓迫等;無癥狀的腦轉移可以入組(放療後至少4 周內沒有進展和 /或手術切除後沒有出現神經癥狀或體征,不需要用糖皮質激素、抗驚 厥藥物或甘露醇治療); |
| 3 | 研究用藥前28 天內進行過系統性化療、根治性/廣泛性放療、靶向治療、 抗腫瘤生物治療(如腫瘤疫苗、細胞因子或生長因子等),或14 天內進行過局部姑息性放療; |
| 4 | 研究用藥前接受過重大手術或發生過嚴重創傷的影響消除不足14 天 (除外7 天內進行過局部麻醉的皮膚或經皮穿刺活檢術且已經恢復的,可以入組); |
| 5 | 研究用藥前14 天內接受過全身應用的皮質類固醇藥物(強的松> 10 mg/ 天或等效劑量)或其他免疫抑製藥物治療; |
| 6 | 有活動性、已知自身免疫性疾病病史,包括但不限於系統性紅斑狼瘡、銀屑病、類風濕性關節炎、炎性腸道疾病、橋本氏甲狀腺炎等,除外: I 型糖尿病、僅通過激素替代治療可以控制的甲狀腺功能減退、無需全身治療的皮膚病(如白癜風)和已控制的乳糜瀉; |
| 7 | 需要用免疫抑製藥物治療的合併症,或需要按具有免疫抑製作用的劑量 (強的松>10mg/日或同類藥物等效劑量)全身治療的合併症;在沒有 活動性自身免疫疾病的情況下,允許吸入或局部使用類固醇和劑量> 10mg/天強的松或同類藥物等效劑量; |
| 8 | 未得到控制的高血壓(收縮壓>140 mmHg 和/或舒張壓>90 mmHg)或 肺動脈高壓或不穩定型心絞痛;給葯前6 個月內有過心肌梗死或進行過 搭橋、支架手術;滿足紐約心臟病協會(NYHA)標準3-4 級的慢性心 力衰竭病史;有臨床意義的瓣膜病;需要治療的嚴重心律失常,包括 QTc 間期≥470 ms(以Fridericia 公式計算);左心室射血分數(LVEF) <50%;給葯前6 個月內腦血管意外(CVA)或短暫性腦缺血發作(TIA) 等; |
| 9 | 合併其他嚴重的內科疾病,包括但不限於:未控制的糖尿病、活動性消 化道潰瘍、活動性出血等; |
| 10 | 現患有需要全身性治療的活動性感染者; |
| 11 | 既往或現患有活動性結核感染者; |
| 12 | 既往有間質性肺病史; |
| 13 | 有癥狀的難以控制的漿膜腔積液如腹腔積液、胸腔積液或心包積液; |
| 14 | 人類免疫缺陷病毒抗體(HIV-Ab)及梅毒螺旋體(TP)陽性;C肝抗體(HCV-Ab)陽性,且C肝病毒RNA 定量>檢測部門正常值上限;B肝病毒表面抗原(HBsAg)陽性,且B肝病毒檢測值>檢測部門正常值 上限; |
| 15 | 既往治療引起的不良反應還未恢復1 級及以下(CTCAE 5.0)(脫髮及化療藥物引起的2 級神經毒性除外); |
| 16 | 以前用過抗PD-1 抗體、抗PD-L1 抗體、抗PD-L2 抗體或抗CTLA-4 抗體治療(或作用於T 細胞協同刺激或檢查點通路的任何其他抗體); |
| 17 | 研究用藥前28 天內使用過活疫苗或減毒疫苗; |
| 18 | 研究用藥前30 天內使用過其他研究藥物治療或研究性器械; |
| 19 | 經詢問有吸毒史或藥物濫用史者; |
| 20 | 既往有明確的神經或精神障礙史,如癲癇、癡呆,依從性差者; |
| 21 | 哺乳期婦女且不同意停止哺乳; |
| 22 | 已知對重組人源化PD-1 單抗或其任何輔料過敏;已知有變態反應性疾病病史或為嚴重過敏體質; |
| 23 | 研究者認為由於其他各種原因不適合參加本臨床研究者。 |
參加醫院和研究者:
| 序號 | 機構名稱 | 主要研究者 | 國家 | 省(州) | 城市 |
| 1 | 中國醫學科學院腫瘤醫院 | 吳令英 | 中國 | 北京 | 北京 |
| 2 | 北京協和醫院 | 張福泉 | 中國 | 北京 | 北京 |
| 3 | 哈爾濱醫科大學附屬腫瘤醫院 | 張雲艷 | 中國 | 黑龍江 | 哈爾濱 |
| 4 | 雲南省腫瘤醫院 | 楊宏英 | 中國 | 雲南 | 昆明 |
| 5 | 浙江省腫瘤醫院 | 朱筧青 | 中國 | 浙江 | 杭州 |
| 6 | 天津市中心婦產醫院 | 曲芃芃 | 中國 | 天津 | 天津 |
| 7 | 新疆醫科大學第一附屬醫院 | 馬彩玲 | 中國 | 新疆 | 烏魯木齊 |
| 8 | 湖南省腫瘤醫院 | 張克強 | 中國 | 湖南 | 長沙 |
| 9 | 新疆醫科大學附屬腫瘤醫院 | 袁建林 | 中國 | 新疆 | 烏魯木齊 |
| 10 | 中南大學湘雅醫院 | 申良方 | 中國 | 湖南 | 長沙 |
| 11 | 安徽省立醫院 | 潘躍銀 | 中國 | 安徽 | 合肥 |
| 12 | 福建省腫瘤醫院 | 馮梅 | 中國 | 福建 | 福州 |
| 13 | 湖北省腫瘤醫院 | 黃奕 | 中國 | 湖北 | 武漢 |
| 14 | 華中科技大學同濟醫學院附屬協和醫院 | 李貴玲 | 中國 | 湖北 | 武漢 |
| 15 | 山東大學齊魯醫院 | 孔北華 | 中國 | 山東 | 濟南 |
| 16 | 山西醫科大學第二醫院 | 郝敏 | 中國 | 山西 | 太原 |
| 17 | 河南省腫瘤醫院 | 成慧君 | 中國 | 河南 | 鄭州 |
| 18 | 中南大學湘雅二院 | 胡春宏 | 中國 | 湖南 | 長沙 |
| 19 | 南通腫瘤醫院 | 何愛琴 | 中國 | 江蘇 | 南通 |
| 20 | 首都醫科大學附屬北京婦產醫院 | 孔為民 | 中國 | 北京 | 北京 |
申辦部門:嘉和生物葯業有限公司
登記號:CTR20190423
友情提示:
您可以在本公眾號首頁回復關鍵詞「免疫療法」、「肺癌」、「胃癌」、「乳腺癌」、「白血病」、「肝癌」、「腸癌」,獲得相關臨床試驗信息。
聲明本公眾號文章內容僅供信息交流使用。如需醫療服務或諮詢意見,請向專業人士與機構尋求幫助。
訪問 www.chinadrugtrials.org.cn 輸入本試驗註冊登記號,可獲得更多詳情。如果您想了解更多新葯臨床研究機會,可點擊左下角「閱讀原文」,或查看公眾號會話界面底部菜單。
About us
點「好看」,分享健康新知