點擊閱讀原文,搶先報名!
本文由醫麥客原創,歡迎分享,轉載須授權
2019年7月27日/醫麥客 eMedClub/--Mustang Bio(納斯達克股票代碼:MBIO),一家臨床階段的生物製藥公司,專註於將細胞和基因療法方面的醫學突破轉化為潛在的方法治療血液系統癌症、實體瘤和罕見的遺傳性疾病。

2019年7月24日,該公司宣布美國食品和藥物管理局(FDA)批準MB-102(CD123 CAR-T)治療急性髓系白血病(AML)孤兒葯指定。FDA先前還授予MB-102 (CD123 CAR-T)孤兒葯稱號,用於治療細胞漿細胞樣樹突狀細胞瘤(BPDCN)。(見推薦閱讀)
推薦閱讀:
目前,MB-102在評估1期劑量遞增臨床試驗的安全性和抗腫瘤活性,評價升級劑量的MB-102患者在複發或難治性AML(組1)和BPDCN(組2)的療效。MB-102在低劑量急性髓系白血病和BPDCN中表現出完全的應答,而沒有劑量限制毒性。
為鼓勵製藥公司開發治療罕見疾病的方法,美國於1983年推出了《孤兒藥物法》(ODA)通過提供如研發補助,稅收減免,免收監管費用,優先評估審批和市場排他等多項激勵措施,促進罕見病新葯的研發。此次的孤兒葯指定,將更加有利於野馬生物後續的研究和未來的商業化。
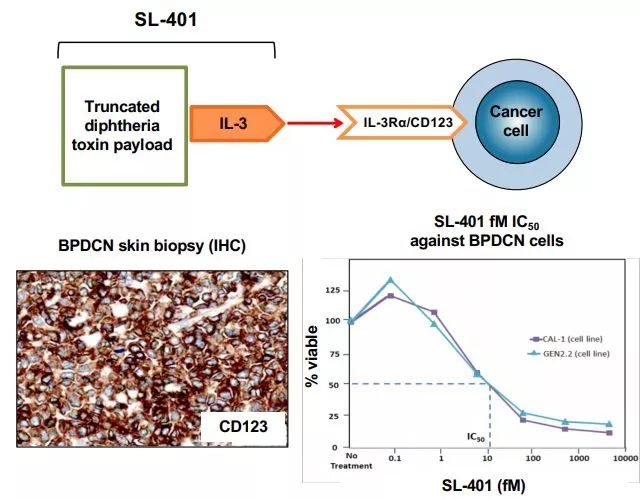
急性髓系白血病是骨髓系血細胞的一種癌症,其主要特徵是異常白細胞的快速生長,這些異常白細胞在骨髓中積聚,干擾正常血細胞的產生。由於CD123在AML中的高表達,CD123是T細胞過繼免疫治療的一個有吸引力的靶點。
MB-102 (CD123 CAR-T)是一種CAR-T細胞療法,用於識別和消除表達CD123的腫瘤。CD123廣泛表達於骨髓增生異常綜合征患者的骨髓細胞以及血液惡性腫瘤中,包括AML、B細胞急性淋巴細胞白血病、毛細胞白血病、BPDCN、慢性髓細胞白血病和霍奇金淋巴瘤。
Manuel Litchman醫學博士說:「我們很高興MB-102獲得了AML和BPDCN兩種適應症的孤兒葯指定。AML最常見於老年人,由於健康狀況,他們中的許多人不得不放棄化療。MB-102有潛力成為這些患者和其他患者的一種重要的新治療方法,並有可能解決多個高度未滿足醫療需求的領域。我們希望在未來幾個月對AML、BPDCN和高危骨髓增生異常綜合征患者開展多中心1/2期臨床試驗。」

管線

該公司其他項目有MB-107,這是一種基因療法,由St Jude兒童研究醫院許可,用於X連鎖嚴重聯合免疫缺陷(X-SCID),也稱為「泡泡男孩」綜合症,正處於1/2期試驗階段。該試驗的數據於4月在新英格蘭醫學雜誌上發表。
2019年5月8日,該公司宣布,在希望之城已開始招募創新性CS1嵌合抗原受體(CAR)治療複發或抵抗性多發性骨髓瘤患者T細胞療法(MB-104)試驗。

▲圖片來源:
雖然到目前為止,Mustang Bio的臨床CAR-T項目和基因治療項目仍沒有上市的產品,但FDA對於其MB-102候選產品的又一孤兒葯指定說明了對這種療法的認可,也許隨著研究的開展未來產品的上市只是時間問題。
推薦閱讀:
ASH重磅:City of Hope公布CD123 CAR-T臨床結果,首例BPDCN患者獲完全緩解丨醫麥猛爆料
關於Mustang Bio
Mustang Bio, Inc.(「Mustang」)是一家臨床階段的生物製藥公司,專註於將當今細胞和基因治療的醫學突破轉化為治療血液癌、實體腫瘤和罕見基因疾病的潛在療法。Mustang的目標是通過許可或以其他方式獲得所有權來獲得這些技術的權利,為研究和開發提供資金,並超過許可或將這些技術推向市場。Mustang已經與頂級醫療機構合作,促進CAR-T和CRISPR/ cas9增強CAR-T治療多種癌症的發展,以及X-SCID的慢病毒基因治療。Mustang根據1934年修訂後的《證券交易法》(Securities Exchange Act of 1934)註冊,並向美國證券交易委員會(sec)提交定期報告。野馬由堡壘生物科技有限公司(NASDAQ: FBIO)創立。
更多信息,請訪問www.mustangbio.com。
參考來源:

醫麥猛爆料