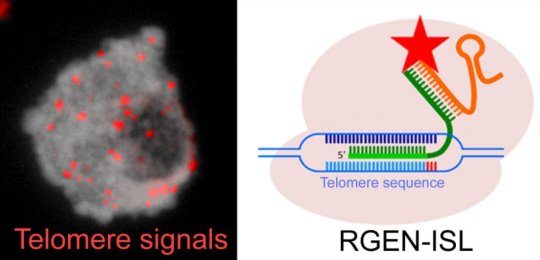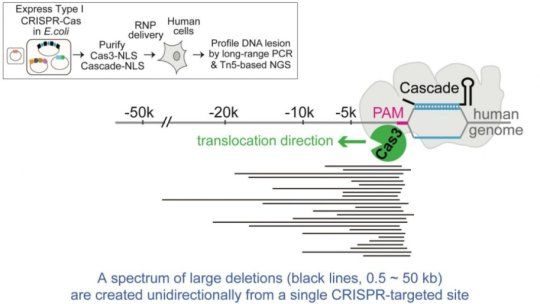

這是一種新技術是如何在人類細胞(上框)中成為可能
在過去的六年裡,一種叫做CRISPR-Cas9的工具已經改變了基因研究,允許科學家在精確的位置像一把小剪刀那樣剪切和編輯DNA鏈。
但有時,做這件事需要的不僅僅是剪刀。現在,一個國際協作團隊已經推出了一種新的基於crispr的工具,它的功能更像一個碎紙機,能夠通過可編程目標清除人類細胞中的長段dna。
寫進帳子細胞他們描述了他們如何成功地獲得了一種不同類型的CRISPR-Cas系統,稱為第一種CRISPR-Cas3型系統,首次在人類細胞中作為遠程DNA編輯工具工作。
生成的工具提供了一種方法來鎖定和刪除比當前Cas9工具更長的DNA。這種力量可以在基因研究中發揮作用,以了解疾病的基礎-並可能用於治療與DNA長段相關的疾病。
領導這項研究的密歇根大學科學家張燕博士解釋說,這一新工具使用的CRISPR系統與廣泛使用的包含Cas9的CRISPR系統不同。兩者都是從細菌中借用的,在細菌中,它們通常會發現並清除入侵的DNA。
一種不同類型的CRISPR
這個新工具使用的是第一類CRISPR,它在細菌中比包含Cas9的II型品種更常見。第一型CRISPR從未用於任何真核細胞,它使用一種名為Cascade的核蛋白複合物來尋找其目標,並使用一種名為Cas3的酶來切割DNA。
這項具有挑戰性的蛋白質優化和純化方面的工作是在康奈爾大學教授艾龍科博士實驗室完成的,他是本論文的共同作者之一。康奈爾大學研究生亞當·多蘭和U-M高級研究專家侯中剛是論文的第一作者。
這項研究涉及張先生(他研究了細菌CRISPR-Cas9並開發了在人體細胞中編輯遺傳物質的工具)和Ke,他用結構和生化方法研究了I型CRISPR。
他們開始嘗試將細菌CRISPR組分作為蛋白質傳遞到人類胚胎乾細胞和另一種叫做HAP 1的細胞中。通過一份CRISPR指南,該團隊成功地刪除了從幾百個鹼基對到100個鹼基的部分目標DNA。
機動碎紙機
張先生稱級聯-Cas3系統為「帶有馬達的dna切碎機」,因為它可以在一定距離內沿DNA基因組移動,隨著時間的推移分解遺傳物質。
「Cas9是一種分子剪刀,你想要它就去哪裡,剪一次,」U-M醫學院生物化學助理教授張說。「但是Cas3會去你想要的地方,沿著染色體傳播,並會產生幾十千位元組長的缺失譜。這可能會使它成為一個強大的篩選工具,用來確定哪些大範圍的DNA對特定疾病最重要。」
當科學家們正在研究「非編碼」的dna的「非編碼」長片段,不包含特定蛋白質的編碼時,這可能特別有用;「碎紙機」技術可以讓他們拆除一系列的長片段,看看會發生什麼。
此外,Cas3在染色體上長距離移動的能力不能用目前的Cas9技術來實現。因此,一個「核酸酶死」版本的Cas3可以沿著dna傳播,但缺乏粉碎功能,這可能為遠距離表觀基因組工程提供一個強大的交付平台。
科學挑戰
研究工作的一部分涉及到如何讓人類乾細胞揭示是否有DNA被刪除,因為大多數用於研究CRISPR-Cas9的乾細胞「報告」系在分解活性低的情況下不夠敏感。澳大利亞墨爾本大學的SaraHowden博士致力於構建一種敏感的雙記者細胞系。
研究小組面臨的另一個挑戰是,利用下一代dna測序,並超越現有的方法,研究cas 9產生的小編輯,找出碎紙機在做了什麼之後碎了什麼。
侯開發了一種基於轉座子酶的分析方法,U-M大學生物化學、計算醫學和生物信息學助理教授PeterFreddolino博士建立了定製的信息學管道來分析深度測序結果。
Ke在論文中還指出,由於指示「碎紙機」所需的引導RNA序列比CRISPR-Cas9系統中使用的序列長,而且由於目標搜索和退化是兩個分離的步驟,因此新方法有可能得到更好的控制。在不需要他們的地方,做出錯誤的削減的可能性可能更小。
這種新的工具及其衍生物可以用於治療目的,張推測,雖然這樣的用途在未來幾年。
一些CRISPR-以Cas9為基礎的治療用途-已經被報導-包括對一個受體基因進行有爭議的編輯,該基因使HIV能夠進入據報導在中國出生的兩個嬰兒胚胎中的細胞。但是對於CRISPR-Cas9在人類DNA正常區域進行非預期編輯的擔憂也浮出水面。還需要進一步研究「碎紙機」辦法是否能避免這一問題。
TAG: |