
作者:Ruthy
數據顯示,目前我國原發性肝癌的發病人數約佔全球55%,因該病死亡的人數已達全球45%-50%,這些觸目驚心的數字為我國醫療事業的發展之路敲響了警鐘。隨著科技的進步,靶向治療應運而生,為肝癌患者帶來了新希望。如何讓這份希望切切實實利好於肝癌患者呢?首要解決的就是靶點問題。近日,西班牙國立心血管病研究中心(CNIC)的研究人員意外發現p38激酶之一——p38γ蛋白是肝縱橫諜海進程啟動和發展的重要調節因子,證明了p38γ可作為肝癌治療的新潛在靶點,為肝癌靶向治療提供了新思路。


--p38γ:意外發現的縱橫諜海調控的關鍵--
該研究成果其實可以算是意外之喜。P38蛋白激酶(p38 MAPK)是絲裂原活化蛋白激酶(MAPKs)亞類之一,其為應激激活的蛋白激酶。目前已發現p38 MAPK有5個異構體,分別為p38α(p38)、p38β1、p38β2、p38γ、p38δ。研究人員最開始的目的是探討該激酶家族在動脈粥樣硬化中的作用,第一步就是先解析這些蛋白的結構。他們對該家族成員和其他蛋白進行三維結構的深入對比分析,發現p38γ與CDK蛋白具有高度相似性。CDK蛋白是細胞周期蛋白依賴性激酶,又被稱作細胞周期引擎,是保證細胞周期不斷運行的關鍵因子。那麼,與CDK蛋白高度相似的p38γ是否也是細胞周期調控的關鍵呢?

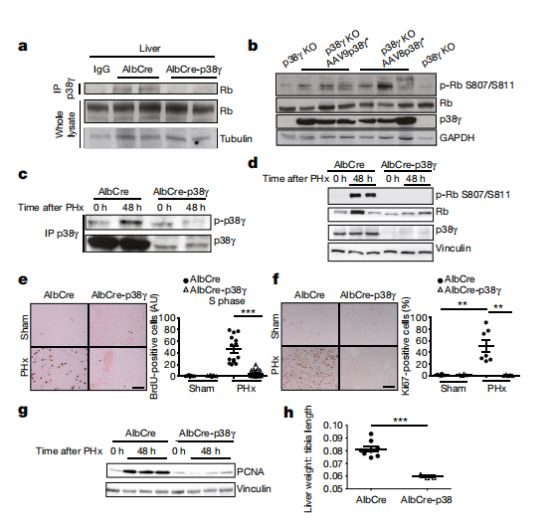
p38γ磷酸化Rb蛋白
後續試驗中,研究人員發現CDK1的抑製分子可同時抑製p38γ,而p38γ可以磷酸化修飾抑癌蛋白Rb,且其修飾的位點與CDK相同。另外,只要敲除p38γ,就可以終止實驗小鼠的Rb磷酸化修飾,這種現象會隨著p38γ的重新引入而消除。Rb是一類DNA結合蛋白,目前已證實在細胞周期的G1期,Rb蛋白被CDK磷酸化後可變成p-Rb,釋放結合在其上的E2F,促進S期所必需的Cyclin、CDK蛋白的轉錄。也就是說,只有Rb成功磷酸化,細胞才能從G1期進入S期,而p38γ在細胞周期中發揮的作用與CDK完全相同,正是細胞周期調控的關鍵!那為什麼會將p38γ的作用與肝癌聯繫起來呢?
--p38γ:與肝癌的發生發展密不可分--
我們知道,p38γ的重要「落腳點」之一就是肝臟。研究人員發現,敲除實驗小鼠的p38γ後,其肝細胞的DNA合成與細胞增殖皆受到明顯抑製,肝細胞的再生也顯著受阻,而這個作用也延續到了肝癌細胞身上。研究人員指出,在人類和動物的肝癌標本中,p38γ的表達皆有較高水準的升高,而這直接關係著肝癌患者的不良預後。他們敲除了肝癌小鼠的p38γ,發現小鼠肝癌細胞的增殖速度明顯變緩,數量減少,同時小鼠的生存期大幅度延長,而且該結果在其他動物模型中皆得到驗證。這就證實了p38γ與肝癌的發生發展密不可分,也就意味著p38γ是肝癌重要的潛在治療靶點!抑製p38γ有望成為肝癌治療的新手段!
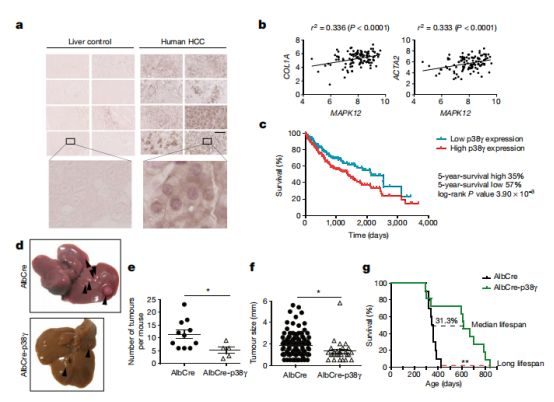
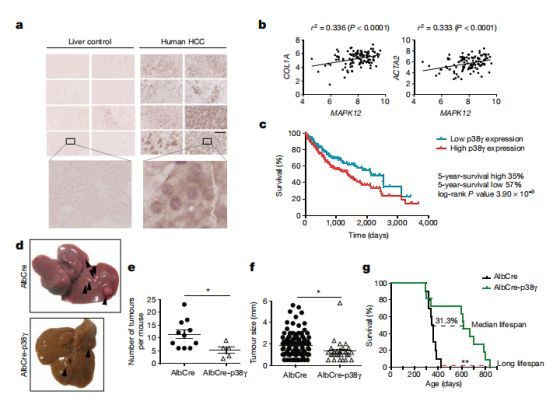
p38γ促進肝癌發展
這項研究無心插柳柳成蔭,意外地讓肝癌新的潛在治療靶點現形,為肝癌靶向治療提供了新思路。另一方面,p38γ對多種細胞周期皆有調控作用,所以,抑製p38γ或許也是其他癌症的全新治療途徑,這對廣大癌症患者來說,是莫大的福音。
參考文獻:
Anto年 Tomás-Loba,et al.p38γ is essential for cell cycle progression and liver tumorigenesis.Nature (2019) .(轉化醫學網360zhyx.com)